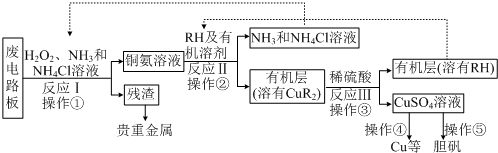
廢舊印刷電路板是一種電子廢棄物,其中銅的含量達到礦石中的幾十倍.濕法技術是將粉碎的印刷電路板經溶解、萃取、電解等操作得到純銅等產品.某化學小組模擬該方法回收銅和制取膽礬,流程簡圖如下:
回答下列問題:
(1)反應Ⅰ是將Cu轉化為Cu(NH3)2+4,反應中H2O2 的作用是作氧化劑作氧化劑.
(2)反應II是銅氨溶液中的Cu(NH3)2+4與有機物RH反應,寫出該反應的離子方程式:Cu(NH3)42++2RH=2NH4++2NH3+CuR2Cu(NH3)42++2RH=2NH4++2NH3+CuR2.操作②用到的主要儀器名稱為分液漏斗分液漏斗,其目的是(填序號)abab.
a.富集銅元素 b.使銅元素與水溶液中的物質分離 c.增加Cu2+在水中的溶解度
(3)操作④以石墨作電極電解CuSO4 溶液.陰極析出銅,陽極產物是O2、H2SO4O2、H2SO4.操作⑤由硫酸銅溶液制膽礬的主要步驟是加熱濃縮、冷卻結晶、過濾加熱濃縮、冷卻結晶、過濾.
(4)流程中有三次實現了試劑的循環使用,已用虛線標出兩處,第三處的試劑是H2SO4H2SO4.
【考點】“三廢”處理與環境保護.
【答案】作氧化劑;Cu(NH3)42++2RH=2NH4++2NH3+CuR2;分液漏斗;ab;O2、H2SO4;加熱濃縮、冷卻結晶、過濾;H2SO4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:22引用:1難度:0.3
相似題
-
1.下列說法不正確的是( )
A.酸雨與土壤中的金屬氧化物反應后,硫元素以硫酸鹽的形式進入土壤中 B.機動車發動機的燃料燃燒時,高溫條件使空氣中的氮氣與氧氣反應,生成氮氧化物 C.節能不是簡單地減少能源的使用,更重要的是要充分有效地利用能源 D.中國天眼傳輸信息用的光導纖維材料的主要成分是硅 發布:2024/12/30 5:30:2組卷:27引用:2難度:0.9 -
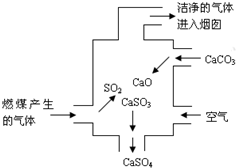 2.右圖是某燃煤發電廠處理廢氣的裝置示意圖.裝置內發生的主要反應中不含( )
2.右圖是某燃煤發電廠處理廢氣的裝置示意圖.裝置內發生的主要反應中不含( )A.化合反應 B.分解反應 C.置換反應 D.氧化還原反應 發布:2024/12/30 4:0:1組卷:331引用:16難度:0.9 -
3.工業上常用微生物法、吸收法、電解法、還原法等消除硫、氮等引起的污染。
(1)微生物法脫硫
富含有機物的弱酸性廢水在SBR細菌作用下產生CH3COOH、H2等物質,可將廢水中還原為H2S,同時用N2或CO2將H2S從水中吹出,再用堿液吸收。SO2-4
①的空間構型為SO2-4.
②CH3COOH與在SBR細菌作用下生成CO2和H2S的離子方程式為SO2-4.
③將H2S從水中吹出時,用CO2比N2效果更好,其原因是.
(2)吸收法脫硫
煙氣中的SO2可以用“亞硫酸銨吸收法”處理,發生的反應為(NH4)2SO3+SO2+H2O═2NH4HSO3,測得25℃時溶液pH與各組分物質的量分數的變化關系如圖-1所示.b點時溶液pH=7,則n():n(NH+4)=HSO-3.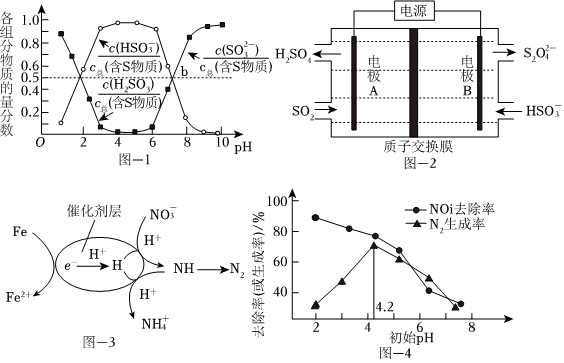
(3)電解法脫硫
用NaOH吸收后SO2,所得NaHSO3溶液經電解后可制取Na2S2O4溶液,反應裝置如圖-2所示。電解時每有1molS2生成有O2-4molH+透過質子交換膜。
(4)還原法脫氮
用催化劑協同納米零價鐵去除水體中。其催化還原反應的過程如圖-3所示。NO-3
①該反應機理中生成N2的過程可描述為.
②過程中去除率及N2生成率如圖-4所示,為有效降低水體中氮元素的含量,宜調整水體pH為4.2,當pH<4.2時,隨pH減小,N2生成率逐漸降低的原因是NO-3。發布:2024/12/30 5:30:2組卷:41引用:4難度:0.5


