幾種主族元素在周期表中的位置如下:
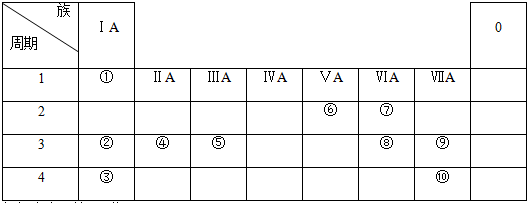
根據上表回答下列問題:
(1)畫出⑩的原子結構示意圖:
 。
。
(2)④和⑨兩種元素形成的化合物的電子式是 
 。
。
(3)②、⑦、⑧三種元素離子半徑由大到小的順序是 S2->O2->Na+S2->O2->Na+(用離子符號表示)。
(4)由⑥、⑨組成的化合物分子中,⑥、⑨原子的最外層均達到8電子穩定結構,該化合物遇水可生成一種具有漂白性的化合物和一種堿性氣體,試寫出該反應的化學方程式:NCl3+3H2O=NH3↑+3HClONCl3+3H2O=NH3↑+3HClO。
(5)對于元素②與④,能說明②的金屬性比④強的是 ACAC(填標號)。
A.②與H2O反應比④與H2O反應劇烈
B.②單質的熔、沸點比④的低
C.②的最高價氧化物對應的水化物的堿性比④的最高價氧化物對應的水化物的堿性強
D.與非金屬單質反應時,②原子失電子數目比④原子失電子數目少
(6)由①、③、⑦組成的化合物中含有的化學鍵有 離子鍵和極性共價鍵離子鍵和極性共價鍵。
(7)在含有①、④、⑤簡單陽離子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到過量,生成沉淀的質量與加入的NaOH溶液的體積關系如圖所示。由圖中數據分析計算:
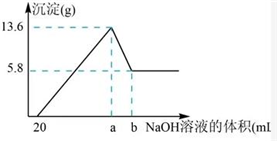
ⅰ.沉淀減少時發生的離子方程式:Al(OH)3+OH-=AlO2-+2H2OAl(OH)3+OH-=AlO2-+2H2O。
ⅱ.a點的數值為 120120mL。




【答案】 ;
; ;S2->O2->Na+;NCl3+3H2O=NH3↑+3HClO;AC;離子鍵和極性共價鍵;Al(OH)3+OH-=AlO2-+2H2O;120
;S2->O2->Na+;NCl3+3H2O=NH3↑+3HClO;AC;離子鍵和極性共價鍵;Al(OH)3+OH-=AlO2-+2H2O;120
 ;
; ;S2->O2->Na+;NCl3+3H2O=NH3↑+3HClO;AC;離子鍵和極性共價鍵;Al(OH)3+OH-=AlO2-+2H2O;120
;S2->O2->Na+;NCl3+3H2O=NH3↑+3HClO;AC;離子鍵和極性共價鍵;Al(OH)3+OH-=AlO2-+2H2O;120【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:18引用:1難度:0.7
相似題
-
1.下列說法正確的是( )
A.元素周期表的d區全部是副族元素 B.元素周期表的d區包含所有的過渡元素 C.過渡元素包括d區、f區、ds區的元素 D.ds區元素不都是副族元素 發布:2024/12/30 19:0:1組卷:3引用:3難度:0.8 -
2.下列關于元素周期表的說法正確的是( )
A.原子序數相差8的兩短周期元素,它們一定是同主族元素 B.外圍電子排布為5s25p4的元素位于第5周期ⅥA族,是p區元素 C.元素周期表每一周期元素原子的最外層電子排布均是從ns1過渡到ns2np6 D.第4周期元素中,基態原子未成對電子數最多的是錳元素 發布:2024/12/30 19:0:1組卷:0引用:3難度:0.7 -
3.元素周期表5個區中都有金屬元素。
(判斷對錯)發布:2024/12/30 19:0:1組卷:2引用:2難度:0.9


