2022-2023學年湖南省長沙一中高一(下)入學化學試卷
發布:2024/12/13 2:0:2
一、選擇題(本題共14小題,每小題3分,共42分。在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.化學與生活密切相關,下列說法不正確的是( )
A.碳酸氫鈉可以做治療胃酸過多的藥物 B.氧化亞鐵常用作油漆的紅色顏料 C.放射性同位素常應用于診斷和治療疾病 D.硬鋁密度小、強度高,是制造飛機和宇宙飛船的理想材料 組卷:8引用:1難度:0.6 -
 2.意大利羅馬大學的一些人獲得了極具理論研究意義的N4分子。N4分子結構如圖所示,下列說法正確的是( )
2.意大利羅馬大學的一些人獲得了極具理論研究意義的N4分子。N4分子結構如圖所示,下列說法正確的是( )A.N4屬于一種新型的化合物 B.N4轉化為N2屬于物理變化 C.N4的摩爾質量為56g D.N4與N2互為同素異形體 組卷:43引用:1難度:0.8 -
3.NA代表阿伏加德羅常數的值。下列說法正確的是( )
A.2g氘化鋰(6LiD)中含中子數為NA B.100g46%的乙醇(C2H5OH)溶液中含有氧原子數為NA C.標準狀況,22.4L由O2與O3組成的混合氣體含有的氧原子數目為NA D.0.2molNa2O2與過量CO2反應時,轉移的電子數為0.4NA 組卷:160引用:1難度:0.7 -
4.如圖裝置(部分夾持裝置省略)所示的實驗方案正確的是( )
A B C D 



制備氫氧化亞鐵 證明非金屬性強弱:Cl>C>Si 驗證碳酸鈉和碳酸氫鈉的穩定性 驗證潮濕氯氣與干燥氯氣的漂白性 A.A B.B C.C D.D 組卷:22引用:1難度:0.5 -
5.下列離子反應方程式正確的是( )
A.氯氣溶于水:Cl2+H2O═2H++Cl-+ClO- B.四氧化三鐵溶于足量硝酸中:Fe3O4+8H+═2Fe3++Fe2++4H2O C.向Fe2(SO4)3溶液中滴入過量Ba(OH)2溶液:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ D.NaHCO3溶液滴入NaHSO4溶液中:HCO3-+H+═H2O+CO2↑ 組卷:328引用:1難度:0.6 -
6.下列描述不正確的是( )
A.37Cl與39K具有相同的中子數 B.第114號元素的一種核素 X與82Pb具有相同的最外層電子數298114C.H3O+與OH-具有相同的質子數和電子數 D. 和S2-具有相同的質子數和電子數O2-2組卷:131引用:3難度:0.6
二、非選擇題(本題共4個小題,共58分)
-
17.Ⅰ.A是一種重要的化工原料,可以制備多種物質。如圖所列物質中,C、D、E均為單質,其中D是一種黃綠色氣體,C在D中燃燒時發出蒼白色火焰,B是一種強堿,焰色試驗火焰呈黃色,H是一種混合物,其水溶液具有漂白性。

(1)A是、F是(以上均寫化學式)。
(2)寫出圖中D生成H的化學方程式:。當反應中消耗0.3molD時,轉移的電子數是。
(3)高溫時,將金紅石(主要成分是TiO2)、焦炭和D混合反應,得到一種可燃性氣體和另一種化合物(由Ti元素和D所含元素組成,其中Ti為+4價,相對分子質量為190)。寫出上述反應的化學方程式:。
Ⅱ.栲膠法脫除煤氣中的硫化氫的工藝流程示意圖如圖:
“吸收”步驟除了生成NaHCO3外,還生成了NaHS,“脫硫”步驟的中間產物可與“吸收”步驟中生成的NaHCO3反應,實現Na2CO3的再生。“氧化Ⅰ”發生反應的化學方程式為Na2V4O9+2NaOH+H2O+Te(醌態)═Te(酚態)+4NaVO3。
(4)NaVO3中V的化合價是。
(5)“氧化Ⅰ”步驟的作用是。
(6)該流程總反應的化學方程式為。組卷:8引用:1難度:0.5 -
18.幾種主族元素在周期表中的位置如下:
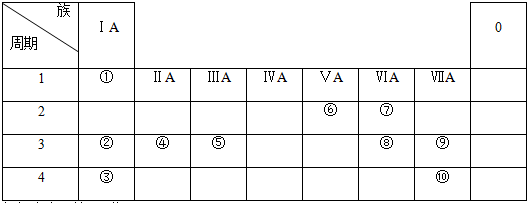
根據上表回答下列問題:
(1)畫出⑩的原子結構示意圖:。
(2)④和⑨兩種元素形成的化合物的電子式是。
(3)②、⑦、⑧三種元素離子半徑由大到小的順序是(用離子符號表示)。
(4)由⑥、⑨組成的化合物分子中,⑥、⑨原子的最外層均達到8電子穩定結構,該化合物遇水可生成一種具有漂白性的化合物和一種堿性氣體,試寫出該反應的化學方程式:。
(5)對于元素②與④,能說明②的金屬性比④強的是(填標號)。
A.②與H2O反應比④與H2O反應劇烈
B.②單質的熔、沸點比④的低
C.②的最高價氧化物對應的水化物的堿性比④的最高價氧化物對應的水化物的堿性強
D.與非金屬單質反應時,②原子失電子數目比④原子失電子數目少
(6)由①、③、⑦組成的化合物中含有的化學鍵有。
(7)在含有①、④、⑤簡單陽離子的100mL溶液中,逐滴滴加5mol/L的NaOH溶液到過量,生成沉淀的質量與加入的NaOH溶液的體積關系如圖所示。由圖中數據分析計算: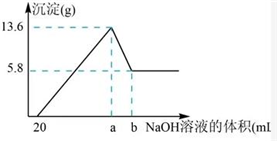
ⅰ.沉淀減少時發生的離子方程式:。
ⅱ.a點的數值為mL。組卷:18引用:1難度:0.7


