研究和深度開發CO,CO2的應用對構建生態文明社會具有重要的意義。
(1)CO可用于煉鐵。
已知:a.Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ?mol-1
b.C(s)+CO2(g)=2CO(g)△H2=+172.5kJ?mol-1
則Fe2O3(s)+3CO(s)═2Fe(s)+3CO2(g)△H=-28.5kJ?mol-1-28.5kJ?mol-1。
(2)CO2和H2充入一定體積的密閉容器中,在兩種溫度下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H,測得CH3OH的物質的量隨時間的變化如圖1所示。
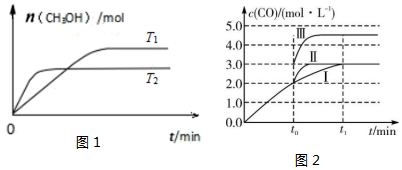
①T1<<T2,△H <<0(填“>”“=”或“<”)。
②一定溫度下,在容積相同且固定的兩個密閉容器中,按如下方式加入反應物,一段時間后達到平衡。
| 容器 | 甲 | 乙 |
| 反應物投入量 | 1molCO2、2molH2 | amolCO2、bmolH2、cmolCH3OH(g)、cmolH2O(g) |
3<C≤1
3<C≤1
。(3)甲醇是重要的化學工業基礎原料和清潔液體燃料。工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如表所示:
| 化學反應 | 平衡常數 | 溫度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
K1?K2
K1?K2
(用K1、K2表示)。500℃時測得反應③在某時刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的濃度(mol?L-1)分別為0.8、0.1、0.3、0.15,則此時v正>
>
(填“>”“=”或“<”)v逆。②在3L容積可變的密閉容器中發生反應②,已知c(CO)隨反應時間t的變化如圖2曲線Ⅰ所示,若在t0時刻分別改變一個條件,曲線Ⅰ變為曲線Ⅱ和曲線Ⅲ。當曲線Ⅰ變為曲線Ⅱ時,改變的條件是
加催化劑
加催化劑
;當曲線Ⅰ變為曲線Ⅲ時,改變的條件是 將容器體積壓縮至2L
將容器體積壓縮至2L
。【答案】-28.5kJ?mol-1;<;<;3<C≤1;K1?K2;>;加催化劑;將容器體積壓縮至2L
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:43引用:1難度:0.3
相似題
-
 1.第五主族的磷單質及其化合物在工業上有廣泛應用.
1.第五主族的磷單質及其化合物在工業上有廣泛應用.
(1)同磷灰石在高溫下制備黃磷的熱化學方程式為:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H已知相同條件下:4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H12Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g)△H2SiO2(s)+CaO(s)=CaSiO3(s)△H3用△H1、△H2和△H3表示△H,則△H=;
(2)白磷與氧氣反應生成P4O10固體.已知斷裂下列化學鍵需要吸收的能量分別為:P-P a kJ?mol-1、P-O b kJ?mol-1、P═O c kJ?mol-1、O═O d kJ?mol-1.根據圖1的分子結構和有關數據通過計算寫出該反應的熱化學方程式為.
(3)三聚磷酸可視為三個磷酸分子(磷酸結構式如圖2)之間脫去兩個水分子產物,其結構式為,三聚磷酸鈉(俗稱“五鈉”)是常用的水處理劑,其化學式為.
(4)次磷酸(H3PO2)為一元酸,分子中含一個羥基,其鈉鹽的正鹽的化學式為,該鹽可用于工業上的化學鍍鎳.①化學鍍鎳的溶液中含有Ni2+和H2PO2-,在酸性等條件下發生下述反應:
(a)□Ni2++□H2PO2-+□=□Ni++□H2PO3-+□
(b)6H2PO-2+2H+=2P+4H2PO3-+3H2↑請在答題卡上寫出并配平反應式(a);
②利用①中反應可在塑料鍍件表面沉積鎳-磷合金,從而達到化學鍍鎳的目的,這是一種常見的化學鍍.請從以下方面比較化學鍍與電鍍.原理上的不同點:;化學鍍的優點:.發布:2024/11/19 8:0:1組卷:77引用:2難度:0.1 -
2.已知在1200℃時,天然氣脫硫工藝中會發生下列反應:
①H2S(g)+O2(g)═SO2(g)+H2O(g) ΔH132
②2H2S(g)+SO2(g)═S2(g)+2H2O(g) ΔH232
③H2S(g)+O2(g)═S(g)+H2O(g) ΔH312
④2S(g)═S2(g) ΔH4
則ΔH4的正確表達式為( )A.ΔH4= (ΔH1+ΔH2-3ΔH3)23B.ΔH4= (3ΔH3-ΔH1-ΔH2)23C.ΔH4= (ΔH1+ΔH2-3ΔH3)32D.ΔH4= (ΔH1-ΔH2-3ΔH3)32發布:2024/12/6 13:30:1組卷:389引用:6難度:0.5 -
3.氨和聯氨(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用.聯氨(又稱肼,N2H4或H2N-NH2,無色液體)是一種應用廣泛的化工原料,可用作火箭燃料.回答下列問題:
(1)聯氨分子的電子式為,其中氮的化合價為;
(2)實驗室中可用次氯酸鈉溶液與氨反應制備聯氨,該反應中還原劑與氧化劑的物質的量之比為2:1,反應的化學方程式為.
(3)①2O2(g)+N2(g)═N2O4(g)△H1
②ON2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=-1038.6kJ?mol-1
上述反應熱效應之間的關系式為△H4=,聯氨和N2O4可作為火箭推進劑的主要原因為.
(4)聯氨可用作火箭燃料,燃燒時發生的反應是N2O4(l)+2N2O4(l)═3N2(g)+4H2O(g)△H=-1038.6kJ?mol-1,若該反應中有4molN-H鍵斷裂,則反應放出的熱量為kJ.發布:2024/11/18 8:0:1組卷:12引用:0難度:0.9


