酸堿中和反應是初中階段重要的一類反應,請你參與一起探究。
【實驗1】從能量變化角度探究酸和堿的反應
某小組同學測量鹽酸與氫氧化鈉溶液反應過程中溫度的變化,觀察到溶液溫度升高,因此,得出兩者能反應的結論。有同學發現此結論不夠嚴謹,在室溫下設計了以下實驗:
①10mL一定濃度的鹽酸與10mL蒸餾水混合,測量溶液溫度的變化。
②10mL一定濃度的氫氧化鈉溶液與10mL蒸餾水混合,測量溶液溫度的變化。
③10mL一定濃度的鹽酸與10mL一定濃度的氫氧化鈉溶液混合,測量溶液溫度的變化。
用數字化實驗技術測得3個實驗,溶液溫度隨時間變化的關系如圖1所示。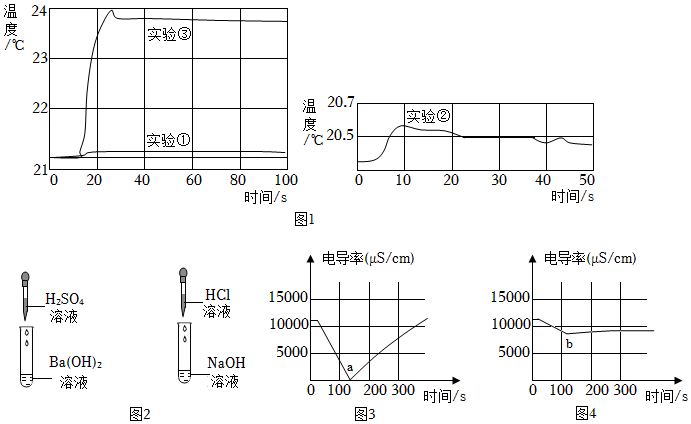
(1)由圖1可知,鹽酸、氫氧化鈉溶液稀釋時均 放熱放熱(填“放熱”或“吸熱”),但它們稀釋時溫度的變化量遠 小于小于(填“大于”或“小于”)兩溶液混合時溫度的變化量。
(2)從微觀角度分析,此中和反應的溫度變化主要是由于 H+、OH-H+、OH-(填離子符號)兩種離子反應放出熱量的緣故,由此說明氫氧化鈉和鹽酸發生了中和反應。
(3)在10mL溶質質量分數為10%NaOH溶液(密度為1.1g/mL)加入溶質質量分數為5%的鹽酸(密度為1.0g/mL)的體積 2020mL,就能使反應后溶液的pH等于7。(結果保留整數)
【實驗2】從溶液電導率變化角度探究酸和堿的反應
小組同學根據圖2進行相應實驗操作,利用電導率傳感器分別測定A試管和B試管反應過程中溶液的電導率變化,電導率的大小能反映離子濃度的大小。
(4)A試管中反應的化學方程式為 H2SO4+Ba(OH)2=BaSO4↓+2H2OH2SO4+Ba(OH)2=BaSO4↓+2H2O;試管B中 無無(填“有”或“無”)明顯現象。
(5)表示A試管中溶液電導率變化的是 圖3圖3(填“圖3”或“圖4”)。
(6)圖4中電導率的變化 能能(填“能”或“不能”)說明酸和堿發生了反應,a點所示溶液中含有的微粒有 H2OH2O(填微粒符號)。
【答案】放熱;小于;H+、OH-;20;H2SO4+Ba(OH)2=BaSO4↓+2H2O;無;圖3;能;H2O
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:161引用:2難度:0.5
相似題
-
1.小明向氫氧化鈉溶液中滴加了稀鹽酸,發現沒有明顯現象。為了判斷兩者是否恰好完全反應,他取少量反應后的溶液加入試管中,滴加幾滴無色酚酞試液,振蕩后觀察到酚酞試液不變色。
(1)根據上述現象,小明得出“兩種物質恰好完全反應”的結論。小白認為小明的結論是不合理的,其理由是。
(2)小白利用pH試紙測反應后溶液的pH,以確定兩者是否恰好完全反應。請你選用其它試劑再設計一個實驗,以驗證氫氧化鈉和鹽酸是否恰好完全反應(要求寫出選用的試劑、可能觀察到的現象和相應的結論)。
(3)小白為了繼續探究“在氫氧化鈉與鹽酸反應的過程中,溶液的pH是如何變化的”這一問題,進行如下實驗:在一定量的氫氧化鈉溶液中逐漸滴加鹽酸,用pH試紙測定溶液的pH,記錄數據如下表:
圖中能合理表示該反應過程中pH變化的圖象是鹽酸的體積/毫升 0 10 19.5 20 20.5 30 40 pH 13 12 11 7 3 2 1 。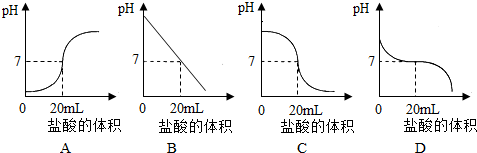 發布:2024/4/20 14:35:0組卷:87引用:18難度:0.5
發布:2024/4/20 14:35:0組卷:87引用:18難度:0.5


