某學生做同主族元素性質遞變規律的實驗時,自己設計了一套實驗方案,并記錄了有關實驗現象.現在請你幫助該學生整理并完成實驗報告.
(1)實驗目的:探究同一主族元素性質的遞變規律探究同一主族元素性質的遞變規律。
(2)實驗用品:藥品:氯水、溴水、溴化鈉溶液、碘化鉀溶液、四氯化碳.儀器:試管、膠頭滴管試管、膠頭滴管。(請填寫兩件主要的玻璃儀器)
(3)實驗內容:
| 序號 | 實驗方案 | 實驗現象 |
|
① |
將少量氯水滴入盛有少量NaBr溶液的試管中,振蕩;再滴入少量四氯化碳,振蕩 | 加入氯水后,溶液由無色變為橙色,滴入四氯化碳后,水層顏色變淺,四氯化碳層(下層)變為橙紅色 |
|
② |
將少量溴水滴入盛有少量KI溶液的試管中,振蕩;再滴入少量四氯化碳,振蕩 | 加入溴水后,溶液由無色變為黃色,滴入四氯化碳后,水層顏色變淺,四氯化碳層(下層)變為紫色 |
同一主族元素,自上而下,元素的非金屬性依次減弱
同一主族元素,自上而下,元素的非金屬性依次減弱
。(5)問題和討論:請用結構理論簡單說明得出上述結論的原因
同一主族元素,自上而下,元素原子的電子層數增多,原子半徑增大,原子核對最外層電子的吸引力逐漸減弱
同一主族元素,自上而下,元素原子的電子層數增多,原子半徑增大,原子核對最外層電子的吸引力逐漸減弱
。【答案】探究同一主族元素性質的遞變規律;試管、膠頭滴管;同一主族元素,自上而下,元素的非金屬性依次減弱;同一主族元素,自上而下,元素原子的電子層數增多,原子半徑增大,原子核對最外層電子的吸引力逐漸減弱
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:35引用:2難度:0.3
相似題
-
1.硅烷是指與烷烴結構類似,分子通式為SinH2n+2的一類化合物.其中一部分烷烴的物理性質如下表:
四種烷烴的物質性質
當n為1時稱為“甲硅烷”,甲硅烷能在空氣中自燃,生成無定形的二氧化硅,同時放出大量的熱.SiH4 Si2H6 Si3H8 Si4H10 熔點(℃) -185 -132.5 -117.4 -84.3 沸點(℃) -111.9 -14.5 52.9 107.4 熔點時密度(g/cm3) 0.68 0.69 0.725 0.79
SiH4+2O2SiO2+2H2O點燃
請完成下列填空:
(1)短周期元素中,原子序數小于硅的主族非金屬元素共有種.短周期元素中,最外層未對電子數與硅相同的元素是(填元素符號).與硅元素同主族的短周期元素A的氫化物與上述化學反應中兩種氫化物比較,穩定性由強到弱的順序是(用化學式表示).
(2)上表中硅烷熔沸點遞變規律是原因是.其中Si3H8的三氯代物分子中極性鍵與非極性鍵的個數比是.
(3)你認為甲硅烷燃燒時除了發光發熱,還可能有的實驗現象是.
(4)硅的最高價含氧酸鈉鹽溶于水,溶液顯性;相同條件下,該溶液與同主族、同濃度的短周期元素A的最高價含氧酸鈉鹽水溶液的pH(填化學式)溶液比溶液大.發布:2024/11/16 8:0:2組卷:38引用:1難度:0.5 -
2.某同學擬通過實驗探究同主族元素性質的遞變規律.設計的實驗方案如下,請你幫他填寫完整,并做出評價.
實驗室提供的試劑:NaBr溶液、NaI溶液、新制的氯水
(1)完善下列實驗報告中的實驗現象和實驗結論.
(2)該同學設計的實驗方案的合理性是實驗步驟 實驗現象 實驗結論 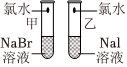
甲: .
乙:溶液由無色變為棕黃色結論:鹵素單質的氧化性由強到弱的順序為Cl2>Br2>I2,請從原子結構的角度解釋: .(填字母).
A.非常合理
B.部分合理
C.完全不合理
(3)上一題(2)中若選A,則此項不用再作答,若選B或C,則完成實驗還需要的試劑是,涉及的離子方程式為.發布:2024/6/27 10:35:59組卷:14引用:1難度:0.6 -
3.下表為元素周期表中的一部分,用化學式或元素符號回答下列問題:
(1)10種元素中,化學性質最不活潑的是族
周期I A ⅡA ⅢA ⅣA VA ⅥA ⅦA 0 2 ⑥ ⑧ 3 ① ③ ⑤ ⑦ ⑩ 4 ② ④ ⑨ ;
(2)④②⑤中,最高價氧化物的水化物,堿性最強的堿是;
(3)②④⑦中形成的簡單離子,半徑由大到小的順序是;
(4)寫出①與⑦形成的最簡單化合物的電子式.
(5)①和⑤最高價氧化物對應的水化物相互反應的化學方程式為
(6)試比較與⑦與⑧兩種元素最簡單氫化物的沸點高低.
(7)設計一個簡單實驗證明⑦⑨兩種元素非金屬性強弱的比較.發布:2024/11/14 8:0:1組卷:17引用:1難度:0.3


