合成氨對人類的生存和發(fā)展有著重要意義,1909年哈伯在實(shí)驗(yàn)室中首次利用氮?dú)馀c氫氣反應(yīng)合成氨,實(shí)現(xiàn)了人工固氮。
(1)反應(yīng)N2(g)+3H2(g)?2NH3(g)的化學(xué)平衡常數(shù)表達(dá)式為 K=c2(NH3)c(N2)×c3(H2)K=c2(NH3)c(N2)×c3(H2)。
(2)請結(jié)合下列數(shù)據(jù)分析,工業(yè)上選用氮?dú)馀c氫氣反應(yīng)固氮,而沒有選用氮?dú)夂脱鯕夥磻?yīng)固氮的原因是 氮?dú)馀c氫氣反應(yīng)的限度遠(yuǎn)遠(yuǎn)大于氮?dú)夂脱鯕夥磻?yīng)的限度氮?dú)馀c氫氣反應(yīng)的限度遠(yuǎn)遠(yuǎn)大于氮?dú)夂脱鯕夥磻?yīng)的限度。
c
2
(
N
H
3
)
c
(
N
2
)
×
c
3
(
H
2
)
c
2
(
N
H
3
)
c
(
N
2
)
×
c
3
(
H
2
)
| 序號 | 化學(xué)反應(yīng) | K(298K)的數(shù)值 |
| ① | N2(g)+O2(g)?2NO(g) | 5×10-31 |
| ② | N2(g)+3H2(g)?2NH3(g) | 4.1×106 |
| 溫度/°C | 壓強(qiáng)MPa | 氨的平衡含量 |
| 200 | 10 | 81.5% |
| 550 | 10 | 8.25% |
放熱
放熱
(填“吸熱”或“放熱”)反應(yīng)。②其他條件不變時(shí),溫度升高氨的平衡含量減小的原因是
B
B
(填字母序號)。A.溫度升高,正反應(yīng)速率減小,逆反應(yīng)速率增大,平衡逆向移動(dòng)
B.溫度升高,K變小。平衡逆向移動(dòng)
C.溫度升高,活化分子數(shù)增多,反應(yīng)速率加快
(4)在合成氨工業(yè)中,原料氣(N2、H2及少量CO、NH3混合氣)在進(jìn)入合成塔前需經(jīng)過銅氨液處理,目的是除去其中的CO,其反應(yīng)為:[Cu(NH3)2]++CO+NH3?[Cu(NH3)3CO]+ΔH<0,則利用銅氨液吸收CO適宜的生產(chǎn)條件是
低溫、高壓
低溫、高壓
。(5)科學(xué)家持續(xù)探索,尋求合成氨的新路徑。如圖為電解法合成氨的原理示意圖,陰極的電極反應(yīng)式為
N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
。
【答案】K=;氮?dú)馀c氫氣反應(yīng)的限度遠(yuǎn)遠(yuǎn)大于氮?dú)夂脱鯕夥磻?yīng)的限度;放熱;B;低溫、高壓;N2+6e-+6H+=2NH3
c
2
(
N
H
3
)
c
(
N
2
)
×
c
3
(
H
2
)
【解答】
【點(diǎn)評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:55引用:1難度:0.7
相似題
-
1.氨既是一種重要的化工產(chǎn)品,又是一種重要的化工原料。如圖為合成氨以及氨催化制硝酸的流程示意圖。下列說法不正確的是( )
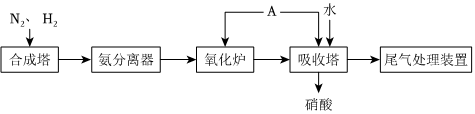
A.可以利用NH3易液化的性質(zhì)分離出NH3 B.吸收塔中通入A是為了提高原料的利用率 C.可以用NH3進(jìn)行氮氧化物的尾氣處理 D.合成氨以及氨催化制硝酸的流程中氮元素均被氧化 發(fā)布:2024/12/30 7:30:1組卷:117引用:7難度:0.7 -
2.2007年諾貝爾化學(xué)獎(jiǎng)授予埃特爾以表彰其對于合成氨反應(yīng)機(jī)理的研究,氮?dú)夂蜌錃夥肿釉诖呋瘎┍砻娴牟糠肿兓^程如圖所示。下列說法不正確的是( )
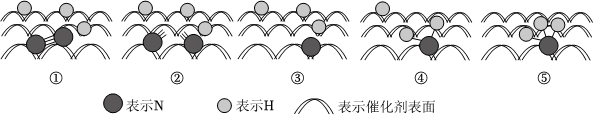
A.圖①→②過程吸熱,圖②→③過程放熱 B.溫度、壓強(qiáng)、催化劑都能改變反應(yīng)的ΔH C.N2在反應(yīng)過程中三鍵均發(fā)生斷裂 D.反應(yīng)過程中存在-NH-、-NH2等中間產(chǎn)物 發(fā)布:2024/11/19 16:0:1組卷:78引用:5難度:0.7 -
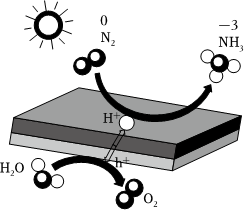 3.光催化固氮合成氨的機(jī)理如圖所示,下列說法不正確的是( )
3.光催化固氮合成氨的機(jī)理如圖所示,下列說法不正確的是( )A.NH3分子是極性分子 B.此反應(yīng)中氮?dú)庾餮趸瘎?/label> C.無論使用哪種催化劑,同一個(gè)反應(yīng)的活化能是不變的 D.此反應(yīng)的化學(xué)反應(yīng)方程式是:2N2+6H2O 4NH3+3O2催化劑光發(fā)布:2024/12/3 18:0:1組卷:74引用:1難度:0.7
相關(guān)試卷


