某實驗小組利用KMnO4酸性溶液與H2C2O4溶液反應研究影響反應速率的因素。設計實驗方案如下(實驗中所用KMnO4溶液均已加入H2SO4):通過測定KMnO4溶液褪色所需時間的多少來比較化學反應速率。為了探究KMnO4與H2C2O4濃度對反應速率的影響,某同學在室溫下完成以下實驗。
| 實驗編號 | 1 | 2 | 3 | 4 |
| 水/mL | 10 | 5 | 0 | X |
| 0.5mol/LH2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/LKMnO4/mL | 5 | 5 | 10 | 10 |
| 時間/S | 40 | 20 | 10 | - |
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
。(2)X=
5
5
,4號實驗中始終沒有觀察到溶液褪色,你認為可能的原因是 KMnO4溶液過量
KMnO4溶液過量
。(3)2號反應中,H2C2O4的反應速率為
0.00625mol/(L?s)
0.00625mol/(L?s)
。(4)在實驗中發現高錳酸鉀酸性溶液和草酸溶液反應時,開始一段時間反應速率較慢,溶液褪色不明顯;但不久突然褪色,反應速率明顯加快。某同學認為是放熱導致溶液溫度升高所致,重做3號實驗,測定過程中溶液不同時間的溫度,結果如下表。
| 時間/S | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 溫度/℃ | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
溫度不是反應速率突然加快的原因
溫度不是反應速率突然加快的原因
。(5)從影響化學反應速率的因素看,你的猜想還可能是
催化劑
催化劑
的影響。若用實驗證明你的猜想,除了酸性高錳酸鉀溶液和草酸溶液外,還需要選擇的試劑最合理的是 D
D
。(填字母)a.硫酸鉀
b.水
c.二氧化錳
d.硫酸錳
【考點】探究影響化學反應速率的因素.
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;5;KMnO4溶液過量;0.00625mol/(L?s);溫度不是反應速率突然加快的原因;催化劑;D
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:26引用:6難度:0.6
相似題
-
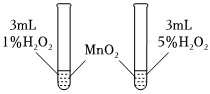 1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )
1.控制變量法是化學實驗的常用方法之一,如圖所示實驗探究影響反應速率的因素是( )A.催化劑 B.溫度 C.濃度 D.壓強 發布:2024/12/30 14:0:1組卷:44引用:3難度:0.6 -
 2.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
2.(一)Fenton法常用于處理含有難降解有機物的工業廢水,通常是在調節好pH和Fe2+濃度的廢水中加入H2O2,所產生的羥基自由基能氧化降解污染物.現運用該方法降解有機污染物p-CP,探究有關因素對該降解反應速率的影響.實驗中控制p-CP的初始濃度相同,恒定實驗溫度在298K或313K下設計如下對比實驗(其余實驗條件見下表):
(1)編號③的實驗目的是實驗序號 實驗目的 T/K pH c/10-3mol?L-1 H2O2 Fe2+ ① 為以下實驗作參照物 298 3 6.0 0.30 ② 探究溫度對降解反應速率的影響 313 3 6.0 0.30 ③ 298 10 6.0 0.30 .
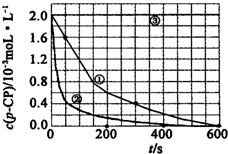
(2)實驗測得不同實驗編號中p-CP的濃度隨時間變化的關系如圖所示.請根據實驗①曲線,計算降解反應在50-300s內的平均反應速率v(p-CP)=.
(3)實驗①②表明,溫度與該降解反應速率的關系是.
(二)已知Fe3+和I-在水溶液中的反應為2I-+2Fe3+=2Fe2++I2.正向反應速率和I-、Fe3+的濃度關系為v=kcm(I-)cn(Fe3+)(k為常數)
(4)請分析下表提供的數據回答以下問題:
①在v=kcm(I-)cn(Fe3+)中,m、n的值為c(I-)/(mol?L-1) c(Fe3+)/(mol?L-1) v/(mol?L-1?s-1) (1) 0.20 0.80 0.032k (2) 0.60 0.40 0.144k (3) 0.80 0.20 0.128k .(選填A、B、C、D)
A.m=1,n=1 B.m=1,n=2 C.m=2,n=1 D.m=2,n=2
②I-濃度對反應速率的影響Fe3+濃度對反應速率的影響(填“<”、“>”或“=”).
(三)一定溫度下,反應FeO(s)+CO(g)?Fe(s)+CO2(g)的化學平衡常數為3.0,該溫度下將2mol FeO、4mol CO、5mol Fe、6mol CO2加入容積為2L的密閉容器中反應.請通過計算回答:
(5)v(正)v(逆)(填“>”、“<”或“=”);若將5mol FeO、4mol CO加入同樣的容器中,在相同溫度下達到平衡,則CO的平衡轉化率為.發布:2024/12/30 14:30:1組卷:20引用:2難度:0.5 -
3.為探究影響化學反應速率的因素,某研究小組設計了如下五個實驗。按要求回答下列問題(已知:Cu2+、Fe3+對H2O2的分解起催化作用)。
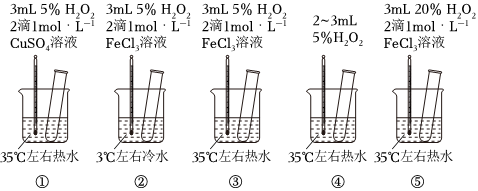
(1)為探究溫度對化學反應速率的影響,應選擇實驗(填序號,下同),選擇的依據是。
(2)為探究催化劑對化學反應速率的影響,同時探究催化劑不同催化效果不同,應選擇實驗。
(3)通過觀察發現實驗⑤比實驗③現象明顯,其原因是。
(4)根據上述實驗,用H2O2快速制取少量O2,可采取的三條措施為。發布:2024/12/30 14:30:1組卷:8引用:5難度:0.5


