(1)實驗室常用紅磷燃燒的方法測定空氣中氧氣的含量(裝置如圖1),寫出紅磷燃燒的文字表達式 紅磷+氧氣點燃五氧化二磷紅磷+氧氣點燃五氧化二磷。
(2)興趣小組同學用家用制氧機(如圖2)制取并收集了一袋氣體,帶到實驗室對其進行研究。家用制氧機的工作原理是用分子篩分離空氣獲得氧氣,分子篩是一種內部分布有均勻微小孔徑的固體,通過特制的分子篩把空氣中的氧分子吸入孔穴而與其它分子分離,該變化屬于 物理物理(填“物理”或“化學”)變化。該方法制得的氧氣濃度如何?
(3)興趣小組同學設計了如圖3所示裝置來測定圖2制氧機制得的氣體中氧氣的含量。請將下列實驗步驟補充完整。
①檢查裝置氣密性。
②加入藥品,將裝置連接固定。
③打開止水夾a和b,向A中緩慢鼓入一定量氣體,關閉止水夾a和b,此時,A中水進入到B中,測得B中水的體積為V1mL。
④用凸透鏡聚光引燃白磷,白磷燃燒,產生大量白煙。
⑤待白磷熄滅并冷卻到室溫,打開止水夾b打開止水夾b(填一操作)。B中水倒吸進入到A中,測得量筒中的體積變為V2mL。
⑥計算小組同學所帶氣體中氧氣的體積分數。
(4)下列有關這個實驗的說法中,正確的有 ACDACD。
A.步驟③中,仰視量筒讀數會使測得的V1數值偏低
B.步驟④中,白磷燃燒時可以不關閉止水夾a和b
C.步驟③中,鼓入的氣體一定要讓白磷露出水面
D.與圖1相比,圖3裝置的優點有:誤差減少和更加環保
(5)通過圖3實驗數據,小組同學算出所帶氣體中氧氣的體積分數為 V1-V2V1×100%V1-V2V1×100%。
點燃
點燃
V
1
-
V
2
V
1
V
1
-
V
2
V
1
【考點】空氣組成的測定;化學變化和物理變化的判別.
【答案】紅磷+氧氣五氧化二磷;物理;打開止水夾b;ACD;×100%
點燃
V
1
-
V
2
V
1
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/7/12 8:0:9組卷:51引用:2難度:0.5
相似題
-
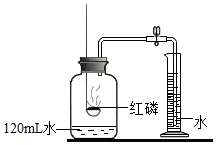 1.用氣密性良好的裝置測定空氣中氧氣的含量。
1.用氣密性良好的裝置測定空氣中氧氣的含量。
(1)紅磷燃燒的化學方程式是。
(2)若使用500mL的集氣瓶,圖中量筒的規格應是(填序號)。
A.20mL
B.50mL
C.100mL
(3)實驗結束后,測得氧氣的體積分數偏小。產生此結果的原因可能是(答1條即可)。發布:2024/12/24 9:30:1組卷:36引用:2難度:0.6 -
2.用如圖裝置測定空氣中氧氣的含量,物質M應該選用( )
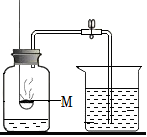
A.鐵片 B.蠟燭 C.木炭 D.紅磷 發布:2024/12/25 12:30:1組卷:10引用:2難度:0.6 -
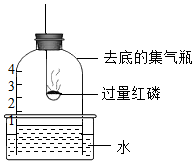 3.用如圖所示裝置進行實驗。下列現象能證明空氣中O2含量的是( )
3.用如圖所示裝置進行實驗。下列現象能證明空氣中O2含量的是( )A.水槽中液面下降 B.紅磷燃燒,產生白煙 C.瓶中液面先下降,后上升 D.瓶中液面最終上升至1處 發布:2024/12/25 13:0:1組卷:243引用:3難度:0.6


