氮是自然界各種生命活動不可缺少的重要元素。
Ⅰ.自然界中氮的循環(如圖所示)
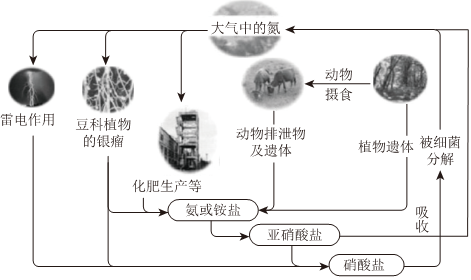
(1)豆科植物的根瘤進行固氮的過程屬于 化學化學(填“化學”或“物理)變化;通過雷電作用進行固氮過程中,第一步反應的化學方程式為 N2+O2 放電 2NON2+O2 放電 2NO。
(2)某氮肥廠產生的氨氮廢水中的氮元素多以NH+4和NH3?H2O的形式存在,設計如圖處理流程:

①過程I:加NaOH溶液,調節pH至9后,升溫至30℃,通入空氣將氨趕出并回收。加入NaOH溶液時,所發生反應的離子方程式為 NH+4+OH- △ NH3+H2ONH+4+OH- △ NH3+H2O。
②過程Ⅱ:在微生物作用下實現NH+4→NO-2→NO-3的轉化,稱為硝化過程。在堿性條件下,NH+4被氧氣氧化為NO-3的總反應的離子方程式為 NH+4+2OH-+2O2=NO-3+3H2ONH+4+2OH-+2O2=NO-3+3H2O。
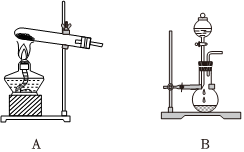
Ⅱ.實驗室制氨氣
(3)實驗室制備氨氣可以選擇A或B裝置,如果選擇A裝置,則發生反應的化學方程式為 Ca(OH)2+2NH4Cl △ CaCl2+2NH3↑+2H2OCa(OH)2+2NH4Cl △ CaCl2+2NH3↑+2H2O;如果選擇B裝置,則分液漏斗中盛裝的物質為 濃氨水濃氨水(填名稱);干燥氨氣時,可選用的干燥劑為 堿石灰或氫氧化鈉堿石灰或氫氧化鈉;收集氨氣采用 向下排空氣法向下排空氣法法。
Ⅲ.濃硝酸和稀硝酸氧化性強弱比較
(4)按如圖所示裝置進行實驗(加持裝置已略去),實驗證明濃硝酸的氧化性強于稀硝酸,依據為濃硝酸能將NO氧化為NO2,而稀硝酸不能。
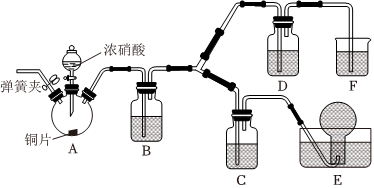
已知:NaOH溶液不與NO反應,能與NO2反應。
①濃硝酸應保存在棕色試劑瓶中,用化學方程式解釋其原因為 4HNO3 光照 4NO2↑+O2↑+2H2O4HNO3 光照 4NO2↑+O2↑+2H2O。
②裝置A中發生反應的化學方程式為 Cu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2OCu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2O;裝置B的作用為 將NO2轉化為NO將NO2轉化為NO。
③裝置D中的現象為 液面上方氣體由無色變為紅棕色液面上方氣體由無色變為紅棕色;C中盛放的試劑為 稀硝酸稀硝酸。
放電
放電
N
H
+
4
NH
+
4
△
NH
+
4
△
N
H
+
4
→
N
O
-
2
→
N
O
-
3
N
H
+
4
N
O
-
3
N
H
+
4
N
O
-
3
N
H
+
4
N
O
-
3
△
△
光照
光照
【考點】含氮物質的綜合應用.
【答案】化學;N2+O2 2NO;+OH- NH3+H2O;+2OH-+2O2=+3H2O;Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O;濃氨水;堿石灰或氫氧化鈉;向下排空氣法;4HNO3 4NO2↑+O2↑+2H2O;Cu+4HNO3(濃)═Cu(NO3)2+2NO2↑+2H2O;將NO2轉化為NO;液面上方氣體由無色變為紅棕色;稀硝酸
放電
NH
+
4
△
N
H
+
4
N
O
-
3
△
光照
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/8/2 8:0:9組卷:44引用:1難度:0.6
相似題
-
1.硫和氮及其化合物在生產生活中應用廣泛,含氮氧化物和硫氧化物的尾氣需處理后才能排放。請回答下列問題:
(1)稀硫酸、稀硝酸與銅粉反應制膽礬晶體,過程中生成一種無色氣體,該氣體是(填化學式),制得的膽礬晶體中可能存在的雜質是(填名稱)。
(2)Na2SO3是實驗室重要的常見藥品,有一瓶放置了很久,小明同學想設計一個實驗驗證這瓶藥品是否變質。請你幫助他設計一個實驗。
(3)一種NH3催化還原NO的物質轉化如圖所示。若參與反應的NH3和O2物質的量之比為4:1,寫出轉化時總反應的化學方程式:。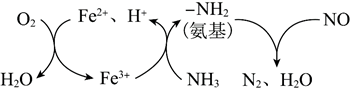
(4)利用氨水可以將SO2和NO2吸收,原理如圖所示: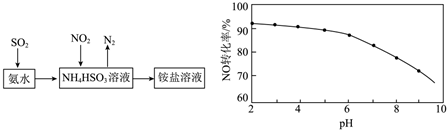
NO2被吸收的離子方程式是。
(5)在酸性NaClO溶液中,HClO氧化NO生成Cl-和。其他條件相同,NO轉化為NO-3的轉化率隨NaClO溶液初始pH(用稀鹽酸調節)的變化如圖所示。NaClO溶液的初始pH越小,NO轉化率越高。其原因是NO-3。發布:2024/12/30 3:30:1組卷:56引用:1難度:0.5 -
2.下列關于自然界中氮循環(如圖)的說法不正確的是( )
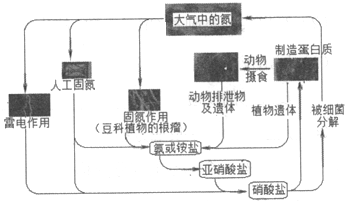
A.人工固氮可以得到硝酸鹽 B.雷電作用可將氮氣直接轉化為銨鹽 C.細菌對氮元素的循環有重要作用 D.亞硝酸鹽轉化為硝酸鹽的過程中,氮元素被氧化 發布:2024/12/30 4:0:1組卷:141引用:2難度:0.9 -
3.下列關于氮的氧化物的說法中正確的是( )
A.氮的氧化物都是酸性氧化物,都是大氣污染物 B.氮的氧化物都既有氧化性,又有還原性 C.NO2與H2O反應生成 HNO3,所以NO2是酸性氧化物 D.可用排空氣法收集NO2 發布:2024/12/30 6:0:2組卷:28引用:2難度:0.5


