氮可以形成多種離子,如N3-,NH-2,N-3,NH+4,N2H+5,N2H2+6等,已知N2H+5與N2H2+6是由中性分子結(jié)合質(zhì)子形成的,類似
于NH+4,因此有類似于 NH+4的性質(zhì).
(1)寫出N2H2+6在堿性溶液中反應(yīng)的離子方程式N2H2+6+2OH-=N2H4+2H2ON2H2+6+2OH-=N2H4+2H2O.
(2)NH-2的電子式為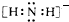
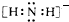 .
.
(3)N-3有2222個電子.
(4)寫出二種由多個原子組成的含有與N-3電子數(shù)相同的物質(zhì)的化學(xué)式N2O、CO2N2O、CO2.
(5)等電子數(shù)的微粒往往具有相似的結(jié)構(gòu),試預(yù)測N-3的構(gòu)型直線型直線型.
(6)據(jù)報道,美國科學(xué)家卡爾?克里斯特于1998年11月合成了一種名為“N5”的物質(zhì),由于其具有極強的爆炸性,又稱為“鹽粒炸彈”.迄今為止,人們對它的結(jié)構(gòu)尚不清楚,只知道“N5”實際上是帶正電荷的分子碎片,其結(jié)構(gòu)是對稱的,5個N排成V形.如果5個N結(jié)合后都達到8電子結(jié)構(gòu),且含有2個N≡N鍵.則“N5”分子碎片所帶電荷是一個單位正電荷一個單位正電荷.
NH
-
2
N
-
3
NH
+
4
H
+
5
H
2
+
6
H
+
5
H
2
+
6
NH
+
4
NH
+
4
H
2
+
6
H
2
+
6
H
2
+
6
NH
-
2
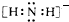
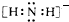
N
-
3
N
-
3
N
-
3
【答案】N2+2OH-=N2H4+2H2O;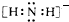 ;22;N2O、CO2;直線型;一個單位正電荷
;22;N2O、CO2;直線型;一個單位正電荷
H
2
+
6
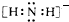 ;22;N2O、CO2;直線型;一個單位正電荷
;22;N2O、CO2;直線型;一個單位正電荷【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:269引用:10難度:0.1
相似題
-
1.根據(jù)VSEPR模型和雜化軌道理論對磷酸根(
)的空間結(jié)構(gòu)的預(yù)測和解釋中,完全正確的是( )PO3-4A.磷酸根離子的空間結(jié)構(gòu)為三角錐形 B.中心原子P的價層電子對數(shù)為4 C.中心原子P的雜化軌道類型為sp3 D.中心原子P的孤電子對數(shù)為1 發(fā)布:2025/1/5 8:0:1組卷:6引用:1難度:0.8 -
2.根據(jù)雜化軌道理論和價層電子對互斥模型判斷,下列說法不正確的是( )
選項 粒子 中心原子雜化方式 VSEPR模型 空間結(jié)構(gòu) A CO2 sp 直線形 直線形 B NH3 sp3 四面體形 三角錐形 C CO2-3sp2 四面體形 平面三角形 D H3O+ sp3 四面體形 三角錐形 A.A B.B C.C D.D 發(fā)布:2025/1/5 8:0:1組卷:78引用:3難度:0.6 -
3.通常把原子總數(shù)和價電子總數(shù)相同的分子或離子稱為等電子體。人們發(fā)現(xiàn)等電子體的空間結(jié)構(gòu)相同,則下列有關(guān)說法中正確的是( )
A.CH4和NH4+是等電子體,鍵角均為60° B.H3O+和PCl3是等電子體,均為平面三角形結(jié)構(gòu) C.NO3-和CO32-是等電子體,均為三角錐形結(jié)構(gòu) D.B3N3H6和苯是等電子體,B3N3H6分子中存在“肩并肩”式重疊的軌道 發(fā)布:2024/12/30 18:0:1組卷:12引用:2難度:0.8


