2014-2015學年山西省運城市康杰中學高二(上)單元測試卷(2)(分子結構與性質)
發布:2024/12/3 16:0:2
一、選擇題(每小題只有一個選項符合題意)
-
1.σ鍵可由兩個原子的s軌道、一個原子的s軌道和另一個原子的p軌道以及一個原子的p軌道和另一個原子的p軌道以“頭碰頭”方式重疊而成.則下列分子中的σ鍵是由一個原子的s軌道和另一個原子的p軌道以“頭碰頭”方式重疊構建而成的是( )
A.H2 B.HCl C.Cl2 D.F2 組卷:47引用:16難度:0.9 -
2.有關乙炔分子中的化學鍵描述不正確的是( )
A.兩個碳原子采用sp雜化方式 B.兩個碳原子采用sp2雜化方式 C.每個碳原子都有兩個未雜化的2p軌道形成π鍵 D.兩個碳原子形成兩個π鍵 組卷:138引用:21難度:0.9 -
3.膦(PH3)又稱磷化氫,在常溫下是一種無色有大蒜臭味的有毒氣體,電石氣的雜質中常含有磷化氫.它的分子構型是三角錐形.以下關于PH3的敘述正確的是( )
A.PH3分子中有未成鍵的孤對電子 B.PH3是非極性分子 C.PH3是一種強氧化劑 D.PH3分子的P-H鍵是非極性鍵 組卷:60引用:26難度:0.9 -
4.碘單質在水溶液中溶解度很小,但在CCl4中溶解度很大,這是因為( )
A.CCl4與I2分子量相差較小,而H2O與I2分子量相差較大 B.CCl4與I2都是直線型分子,而H2O不是直線型分子 C.CCl4和I2都不含氫元素,而H2O中含有氫元素 D.CCl4和I2都是非極性分子,而H2O是極性分子 組卷:283引用:46難度:0.7 -
5.下列事實中能證明氯化氫是共價化合物的是( )
A.液態氯化氫不導電 B.氯化氫極易溶于水 C.氯化氫不易分解 D.氯化氫溶液可以電離 組卷:22引用:4難度:0.7 -
6.下列現象與氫鍵有關的是( )
①HF的熔、沸點比第ⅦA族其他元素氫化物的熔、沸點高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液態水的密度小
④尿素的溶、沸點比醋酸的高
⑤鄰羥基苯甲醛的熔、沸點比對羥基苯甲醛的低
⑥水分子在較高溫度下也很穩定.A.①②③④⑤⑥ B.僅①②③④⑤ C.僅①②③④ D.僅①②③ 組卷:176引用:23難度:0.9 -
7.下列說法不正確的是( )
A.元素的第一電離能(I1)是元素的單質失去最外層1個電子所需要吸收的能量,同周期從左到右元素的I1逐漸增大 B.元素的電負性是衡量元素在化合物中吸引電子能力大小的一種標度,同主族從上到下元素的電負性逐漸減小 C.含有陰離子的晶體中一定含有陽離子,含有陽離子的晶體中不一定含有陰離子 D.原子晶體中一定含有共價鍵;離子晶體中一定含有離子鍵,可能含有共價鍵;分子晶體中一定存在分子間作用力 組卷:15引用:3難度:0.9 -
8.已知X、Y元素同周期,且電負性X>Y,下列說法錯誤的是( )
A.X與Y形成化合物是,X可以顯負價,Y顯正價 B.第一電離能可能Y小于X C.最高價含氧酸的酸性:X對應的酸性弱于Y對應的 D.氣態氫化物的穩定性:HmY小于HmX 組卷:139引用:41難度:0.9 -
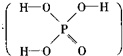 9.已知磷酸分子中的三個氫原子都可以跟重水分子(D2O)中的D原子發生氫交換.又知次磷酸(H3PO2)也可跟D2O進行氫交換,但次磷酸鈉(NaH2PO2)卻不能跟D2O發生氫交換.由此可推斷出H3PO2的分子結構是( )
9.已知磷酸分子中的三個氫原子都可以跟重水分子(D2O)中的D原子發生氫交換.又知次磷酸(H3PO2)也可跟D2O進行氫交換,但次磷酸鈉(NaH2PO2)卻不能跟D2O發生氫交換.由此可推斷出H3PO2的分子結構是( )A. 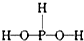
B. 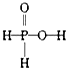
C. 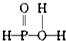
D. 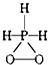 組卷:706引用:41難度:0.7
組卷:706引用:41難度:0.7
三、填空題
-
26.W、X、Y、Z四種元素的原子序數依次增大.其中Y原子的L電子層中,成對電子與未成對電子占據的軌道數相等,且無空軌道;X原子的L電子層中未成對電子數與Y相同,但還有空軌道;W、Z的原子序數相差10,且Z原子的第一電離能在同周期中最低.
(1)寫出下列元素的元素符號:W,X,Y,Z.
(2)XY分子中,X原子與Y原子都達到8電子穩定結構,則XY分子中X和Y原子用于成鍵的電子數目分別是;根據電子云重疊方式的不同,分子里共價鍵的主要類型有.
(3)XY2與ZYW反應時,通過控制反應物的物質的量之比,可以得到不同的產物,相同條件下,在水中溶解度較小的產物是(寫化學式),其原因是該化合物陰離子間可形成二聚離子或多聚鏈狀離子.該化合物陰離子能夠相互締合的原因是:.組卷:24引用:5難度:0.3 -
27.(1)下列物質中,哪些形成分子內氫鍵,哪些形成分子間氫鍵?(填序號)
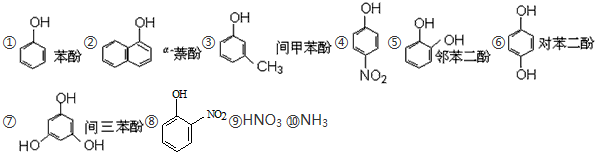
形成分子內氫鍵的有;形成分子間氫鍵有
(2)二聚甲酸解聚反應為:(HCOOH)2→2HCOOH,該反應需吸收60kJ.mol-1的能量,此能量是斷開鍵所需的能量,所以此鍵的鍵能為kJ.mol-1.
(3)氫鍵一般用X-H…Y表示.根據氫鍵形成的條件,可以推測還有元素的原子可以代替氫原子而形成類似氫鍵的結構.組卷:127引用:1難度:0.5


