興趣小組欲用NaOH固體配制溶質質量分數為10%的NaOH溶液100g,用于制作“葉脈書簽”。回答下列問題:

(1)為完成實驗,如圖1除上述儀器外,還須用到的儀器名稱是 玻璃棒玻璃棒,它的主要作用是 攪拌,加速溶解攪拌,加速溶解。該實驗需要稱取NaOH固體的質量為 1010g。
(2)同學A稱量NaOH固體質量之前,先用托盤天平稱量燒杯的質量。稱量時,他把燒杯和砝碼的位置放反了,天平平衡后,砝碼的總和是40g,游碼的位置如圖2所示,則燒杯的實際質量為 37.337.3g。
(3)同學B用正確的方法稱量NaOH固體時,發現天平指針向右偏,則接下來應該 繼續添加氫氧化鈉固體繼續添加氫氧化鈉固體直到天平平衡。
(4)若用溶質質量分數為16%的NaOH溶液配制100g10%的NaOH溶液,則需要16%的NaOH溶液的質量為 62.5g62.5g。
【考點】濃溶液稀釋配制一定質量分數溶液;稱量器-托盤天平.
【答案】玻璃棒;攪拌,加速溶解;10;37.3;繼續添加氫氧化鈉固體;62.5g
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:22引用:1難度:0.6
相似題
-
1.關于配制50g 8%的氫氧化鈉溶液,下列說法正確的是( )
A.用量筒量取50.00mL水 B.將氫氧化鈉固體放在小燒杯中稱量 C.把稱量好的氫氧化鈉固體放入量筒中溶解 D.配制好的溶液存放在帶玻璃塞的廣口瓶中 發布:2024/11/14 23:30:4組卷:220引用:10難度:0.6 -
 2.水是生命之源,揚州是運河之城,也是南水北調的起點.請根據題意回答下列有關水溶液的問題.
2.水是生命之源,揚州是運河之城,也是南水北調的起點.請根據題意回答下列有關水溶液的問題.
(一)將10克NaOH固體完全溶解在40毫升水中(水的密度為1g/cm3),所配溶液中溶質的質量分數為.某同學在配制過程中,量取水時仰視讀數(其它操作均正確),其所配氫氧化鈉溶液中溶質的質量分數將(填“偏大”或“偏小”).另一位同學稱取NaOH時,由于操作不熟練,花了較長時間,那么,他所配氫氧化鈉溶液中溶質的質量分數將.(填“偏大”或“偏小”).
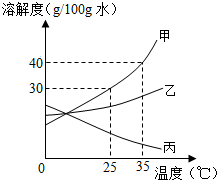
(二)甲、乙、丙三種固體物質的溶解度曲線如圖所示,請回答:
(1)25℃時,將25g甲固體加入到50g水中,充分溶解并恢復到原溫度后,得到溶液的質量為g.
(2)要使35℃時接近飽和的甲溶液變成該溫度下的飽和溶液,可采用的一種方法是.
(3)現有操作步驟:a.溶解 b.過濾 c.降溫結晶 d.加熱濃縮.若甲固體中含有少量乙,則提純甲的操作步驟是(填字母序號).
(4)將35℃時丙的飽和溶液降溫到25℃,則其溶液的溶質質量分數(填“變大”、“變小”或“不變”).
(5)向100g35℃的水中加入48g甲固體,發現全部溶解,一段時間后又有部分甲的晶體析出.你認為“全部溶解”的原因可能是.發布:2024/12/5 8:0:1組卷:30引用:1難度:0.3 -
 3.水是生命之源,揚州是運河之城,也是南水北調的起點。請根據題意回答下列有關水溶液的問題。
3.水是生命之源,揚州是運河之城,也是南水北調的起點。請根據題意回答下列有關水溶液的問題。
(一)將10克NaOH固體完全溶解在40毫升水中(水的密度為1g/cm3),所配溶液中溶質的質量分數為。某同學在配制過程中,量取水時仰視讀數(其它操作均正確),其所配氫氧化鈉溶液中溶質的質量分數將(填“偏大”或“偏小”)。另一位同學稱取NaOH時,由于操作不熟練,花了較長時間,那么,他所配氫氧化鈉溶液中溶質的質量分數將。(填“偏大”或“偏小”)。
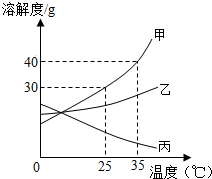
(二)甲、乙、丙三種固體物質的溶解度曲線如圖所示,請回答:
(1)25℃時,將25g甲固體加入到50g水中,充分溶解并恢復到原溫度后,得到溶液的質量為g。
(2)要使35℃時接近飽和的甲溶液變成該溫度下的飽和溶液,可采用的一種方法是。
(3)現有操作步驟:a.溶解 b.過濾 c.降溫結晶 d.加熱濃縮。若甲固體中含有少量乙,則提純甲的操作步驟是(填字母序號)。
(4)將35℃時丙的飽和溶液降溫到25℃,則其溶液的溶質質量分數(填“變大”、“變小”或“不變”)。
(5)向100g35℃的水中加入48g甲固體,發現全部溶解,一段時間后又有部分甲的晶體析出。你認為“全部溶解”的原因可能是。發布:2024/12/5 8:0:1組卷:35引用:1難度:0.5


