鈉離子電池被認(rèn)為在基于電網(wǎng)的儲(chǔ)能系統(tǒng)中最具發(fā)展前景,雙金屬硫化物Sb2S3@FeS2空心納米棒將有助于提高鈉離子電池性能。回答下列問(wèn)題:
(1)Sb位于第五周期,與N同主族,基態(tài)Sb的價(jià)電子排布圖(軌道表達(dá)式)為 
 ,[H2F]+[SbF6]-(氟銻酸)是一種超強(qiáng)酸,[H2F]+的空間構(gòu)型為 V形V形,與[H2F]+具有相同空間構(gòu)型和鍵合形式的陰離子為 NH2-NH2-。
,[H2F]+[SbF6]-(氟銻酸)是一種超強(qiáng)酸,[H2F]+的空間構(gòu)型為 V形V形,與[H2F]+具有相同空間構(gòu)型和鍵合形式的陰離子為 NH2-NH2-。
(2)Si、P與S是同周期中相鄰的元素,Si、P、S的第一電離能由大到小的順序是 P>S>SiP>S>Si。
(3)與S同主族的元素有O、Se、Te等,它們氫化物的沸點(diǎn)大小為H2O>H2Te>H2Se>H2S,其原因是 H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高。
(4)已知:r(Fe2+)為61pm,r(Co2+)為65pm。在隔絕空氣條件下分別加熱FeCO3和CoCO3,實(shí)驗(yàn)測(cè)得FeCO3的分解溫度低于CoCO3,原因是 Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解。
(5)其離子型鐵的氧化物晶胞如圖所示,它由X、Y組成,則該氧化物的化學(xué)式為 Fe3O4Fe3O4;已知該晶體的密度為dg?cm-3,阿伏加德羅常數(shù)的值為NA,則該晶體的晶胞參數(shù)a=3232×8dNA×10-103232×8dNA×10-10pm(用含d和NA的代數(shù)式表示)。



3
232
×
8
d
N
A
3
232
×
8
d
N
A
【考點(diǎn)】同一主族內(nèi)元素性質(zhì)遞變規(guī)律的探究實(shí)驗(yàn);判斷簡(jiǎn)單分子或離子的構(gòu)型;同一主族內(nèi)元素性質(zhì)遞變規(guī)律與原子結(jié)構(gòu)的關(guān)系;晶胞的計(jì)算.
【答案】 ;V形;NH2-;P>S>Si;H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高;Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解;Fe3O4;×10-10
;V形;NH2-;P>S>Si;H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高;Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解;Fe3O4;×10-10
 ;V形;NH2-;P>S>Si;H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高;Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解;Fe3O4;
;V形;NH2-;P>S>Si;H2Te、H2Se、H2S均是分子晶體,相對(duì)分子質(zhì)量逐漸減小,范德華力減小,所以沸點(diǎn)逐漸降低,而水分子間存在氫鍵,所以沸點(diǎn)最高;Fe2+的半徑小于Co2+,F(xiàn)eO的晶格能大于CoO,F(xiàn)eCO3比CoCO3易分解;Fe3O4;3
232
×
8
d
N
A
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:73引用:3難度:0.3
相似題
-
1.硅烷是指與烷烴結(jié)構(gòu)類似,分子通式為SinH2n+2的一類化合物.其中一部分烷烴的物理性質(zhì)如下表:
四種烷烴的物質(zhì)性質(zhì)
當(dāng)n為1時(shí)稱為“甲硅烷”,甲硅烷能在空氣中自燃,生成無(wú)定形的二氧化硅,同時(shí)放出大量的熱.SiH4 Si2H6 Si3H8 Si4H10 熔點(diǎn)(℃) -185 -132.5 -117.4 -84.3 沸點(diǎn)(℃) -111.9 -14.5 52.9 107.4 熔點(diǎn)時(shí)密度(g/cm3) 0.68 0.69 0.725 0.79
SiH4+2O2SiO2+2H2O點(diǎn)燃
請(qǐng)完成下列填空:
(1)短周期元素中,原子序數(shù)小于硅的主族非金屬元素共有種.短周期元素中,最外層未對(duì)電子數(shù)與硅相同的元素是(填元素符號(hào)).與硅元素同主族的短周期元素A的氫化物與上述化學(xué)反應(yīng)中兩種氫化物比較,穩(wěn)定性由強(qiáng)到弱的順序是(用化學(xué)式表示).
(2)上表中硅烷熔沸點(diǎn)遞變規(guī)律是原因是.其中Si3H8的三氯代物分子中極性鍵與非極性鍵的個(gè)數(shù)比是.
(3)你認(rèn)為甲硅烷燃燒時(shí)除了發(fā)光發(fā)熱,還可能有的實(shí)驗(yàn)現(xiàn)象是.
(4)硅的最高價(jià)含氧酸鈉鹽溶于水,溶液顯性;相同條件下,該溶液與同主族、同濃度的短周期元素A的最高價(jià)含氧酸鈉鹽水溶液的pH(填化學(xué)式)溶液比溶液大.發(fā)布:2024/11/16 8:0:2組卷:38引用:1難度:0.5 -
2.下表為元素周期表中的一部分,用化學(xué)式或元素符號(hào)回答下列問(wèn)題:
(1)10種元素中,化學(xué)性質(zhì)最不活潑的是族
周期I A ⅡA ⅢA ⅣA VA ⅥA ⅦA 0 2 ⑥ ⑧ 3 ① ③ ⑤ ⑦ ⑩ 4 ② ④ ⑨ ;
(2)④②⑤中,最高價(jià)氧化物的水化物,堿性最強(qiáng)的堿是;
(3)②④⑦中形成的簡(jiǎn)單離子,半徑由大到小的順序是;
(4)寫出①與⑦形成的最簡(jiǎn)單化合物的電子式.
(5)①和⑤最高價(jià)氧化物對(duì)應(yīng)的水化物相互反應(yīng)的化學(xué)方程式為
(6)試比較與⑦與⑧兩種元素最簡(jiǎn)單氫化物的沸點(diǎn)高低.
(7)設(shè)計(jì)一個(gè)簡(jiǎn)單實(shí)驗(yàn)證明⑦⑨兩種元素非金屬性強(qiáng)弱的比較.發(fā)布:2024/11/14 8:0:1組卷:17引用:1難度:0.3 -
3.某同學(xué)擬通過(guò)實(shí)驗(yàn)探究同主族元素性質(zhì)的遞變規(guī)律.設(shè)計(jì)的實(shí)驗(yàn)方案如下,請(qǐng)你幫他填寫完整,并做出評(píng)價(jià).
實(shí)驗(yàn)室提供的試劑:NaBr溶液、NaI溶液、新制的氯水
(1)完善下列實(shí)驗(yàn)報(bào)告中的實(shí)驗(yàn)現(xiàn)象和實(shí)驗(yàn)結(jié)論.
(2)該同學(xué)設(shè)計(jì)的實(shí)驗(yàn)方案的合理性是實(shí)驗(yàn)步驟 實(shí)驗(yàn)現(xiàn)象 實(shí)驗(yàn)結(jié)論 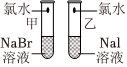
甲: .
乙:溶液由無(wú)色變?yōu)樽攸S色結(jié)論:鹵素單質(zhì)的氧化性由強(qiáng)到弱的順序?yàn)镃l2>Br2>I2,請(qǐng)從原子結(jié)構(gòu)的角度解釋: .(填字母).
A.非常合理
B.部分合理
C.完全不合理
(3)上一題(2)中若選A,則此項(xiàng)不用再作答,若選B或C,則完成實(shí)驗(yàn)還需要的試劑是,涉及的離子方程式為.發(fā)布:2024/6/27 10:35:59組卷:14引用:1難度:0.6


