25℃時,在體積為2L的密閉容器中,氣態物質A、B、C的物質的量n隨時間t的變化如圖1所示,已知達平衡后,降低溫度,A的轉化率將增大。

(1)根據圖中數據,寫出該反應的化學方程式 A(g)+2B(g) 2C(g)A(g)+2B(g)
2C(g)A(g)+2B(g) 2C(g);此反應的平衡常數表達式K=c2(C)c(A)?c2(B)c2(C)c(A)?c2(B)。
2C(g);此反應的平衡常數表達式K=c2(C)c(A)?c2(B)c2(C)c(A)?c2(B)。
(2)0~3min,v(C) 0.10.1mol?L-1?min-1。
(3)在5~7min內,若K值不變,則此處曲線變化的原因是 增大壓強增大壓強。
(4)如圖2表示此反應的反應速率v和時間t的關系圖,各階段的平衡常數如表所示:
 2C(g)
2C(g) 2C(g)
2C(g)c
2
(
C
)
c
(
A
)
?
c
2
(
B
)
c
2
(
C
)
c
(
A
)
?
c
2
(
B
)
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |
K1>K2=K3=K4
K1>K2=K3=K4
;A的轉化率最大的一段時間是 t2~t3
t2~t3
。【考點】物質的量或濃度隨時間的變化曲線.
【答案】A(g)+2B(g) 2C(g);;0.1;增大壓強;K1>K2=K3=K4;t2~t3
2C(g);;0.1;增大壓強;K1>K2=K3=K4;t2~t3
 2C(g);
2C(g);c
2
(
C
)
c
(
A
)
?
c
2
(
B
)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:9引用:4難度:0.6
相似題
-
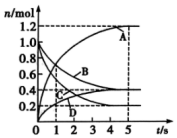 1.一定溫度下,向容積為2L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如圖所示。則下列對該反應的推斷合理的是( )
1.一定溫度下,向容積為2L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如圖所示。則下列對該反應的推斷合理的是( )A.該反應的化學方程式為6A+2D?3B+4C B.0~1s內,v(A)=v(B) C.5s時,v(A)=v(B)=v(C)=v(D) D.0~5s內,B的平均反應速率為0.06mol/(L?s) 發布:2024/12/30 19:30:2組卷:32引用:3難度:0.7 -
2.一定溫度下,在容積為2L的密閉容器中,與同一個化學反應有關的A、B、C、D(其中A、B、C均為氣體)四種物質的物質的量隨反應時間的變化如圖所示。E為該反應的另一種氣態生成物,且在化學方程式中E的化學計量數與B的相同。請回答下列問題:
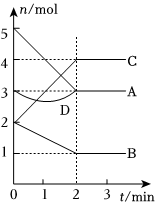
(1)該反應的反應物為。
(2)0~2min內,v(C)=,v(E)=。
(3)若降低溫度,則v(正)(填“加快”、“減慢”或“不變”,下同),v(逆)。
(4)該反應達到平衡狀態的標志有。(填序號)
a.A和C的物質的量相等
b.B的物質的量保持不變
c.A的正反應速率與B的逆反應速率之比為2:1
d.容器內壓強不變
(5)物質D在反應中的作用是。發布:2024/12/30 14:30:1組卷:10引用:3難度:0.7 -
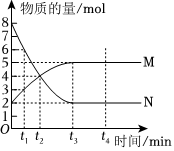 3.一定溫度下,在容積為VL的密閉容器中進行反應:aN(g)?bM(g),M、N的物質的量隨時間的變化曲線如圖所示,下列說法錯誤的是( )
3.一定溫度下,在容積為VL的密閉容器中進行反應:aN(g)?bM(g),M、N的物質的量隨時間的變化曲線如圖所示,下列說法錯誤的是( )A.此反應的化學方程式中a:b=2:1 B.t3時刻該反應達到化學平衡 C.當混合氣體的總質量不隨時間的變化而變化時反應達到平衡狀態 D.任意時刻都滿足v(N)正=2v(M)正 發布:2024/12/30 14:30:1組卷:17引用:2難度:0.7


