工廠煙氣(主要污染物SO2、NO)直接排放會造成空氣污染,需處理后才能排放。
(1)O3氧化。O3氧化過程中部分反應的能量變化如圖1所示。

①已知2SO2(g)+O2(g)=2SO3(g) ΔH=-198 kJ?mol-1。則反應2O3(g)=3O2(g)的ΔH=-285.2-285.2kJ?mol?1。
②其他條件不變時,增加n(O3),O3氧化SO2的反應幾乎不受影響,其可能原因是 SO2與O3反應的活化能比NO與O3反應的活化能大得多,其他條件不變時SO2與O3的反應速率慢SO2與O3反應的活化能比NO與O3反應的活化能大得多,其他條件不變時SO2與O3的反應速率慢。
(2)“納米零價鐵-H2O2”體系可將煙氣中難溶的NO氧化為可溶的NO-3。在一定溫度下,將H2O2溶液和HCl溶液霧化后與煙氣按一定比例混合,以一定流速通過裝有納米零價鐵的反應裝置,可將煙氣中的NO氧化。
①Fe2+催化H2O2分解產生HO?,HO?將NO氧化為NO-3的機理如圖2所示,Y的化學式為 Fe3+或FeCl3Fe3+或FeCl3。
②NO與H2O2反應生成HNO3的化學方程式為 2NO+3H2O2=2HNO3+2H2O2NO+3H2O2=2HNO3+2H2O。
③納米零價鐵的作用是 與HCl溶液反應產生Fe2+與HCl溶液反應產生Fe2+。
④NO脫除率隨溫度的變化如圖3所示。溫度高于120℃時,NO脫除率隨溫度升高呈現下降趨勢的主要原因是 H2O2的分解速率隨溫度升高而加快,H2O2濃度減小,NO脫除率降低H2O2的分解速率隨溫度升高而加快,H2O2濃度減小,NO脫除率降低。
NO
-
3
NO
-
3
【考點】反應熱和焓變;氮的氧化物的性質及其對環境的影響.
【答案】-285.2;SO2與O3反應的活化能比NO與O3反應的活化能大得多,其他條件不變時SO2與O3的反應速率慢;Fe3+或FeCl3;2NO+3H2O2=2HNO3+2H2O;與HCl溶液反應產生Fe2+;H2O2的分解速率隨溫度升高而加快,H2O2濃度減小,NO脫除率降低
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:109引用:2難度:0.5
相似題
-
1.下列說法不正確的是( )
A.CH3COOH 溶液加水稀釋后,溶液中 的值減小c(CH3COOH)c(CH3COO-)B.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為α,Ka= .若加入少量醋酸鈉固體,則CH3COOH?CH3COO-+H+向左移動,α減小,Ka變小(cα)2c(1-α)C.實驗測得環己烷(l)、環己烯(l)和苯(l)的標準燃燒熱分別為-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以證明在苯分子中不存在獨立的碳碳雙鍵 D.已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol.
CO(g)+O2(g)═CO2(g),△H=-283.0 kJ/mol.12
C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol.
則4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol發布:2025/1/1 8:0:2組卷:11引用:1難度:0.7 -
2.下列與化學反應的能量變化有關的敘述正確的是( )
A.由石墨比金剛石穩定可知,C(金剛石)═C(石墨)△H<0 B.一個反應的反應物的總能量可能等于其生成物的總能量 C.有熱量變化的反應一定是化學反應 D.強酸與強堿的中和反應的熱化學方程式均可表示為H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1 發布:2025/1/6 6:0:5組卷:1引用:3難度:0.6 -
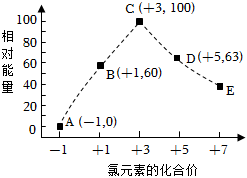 3.一定條件下,在水溶液中物質的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩定的點為( )
3.一定條件下,在水溶液中物質的量均為1mol的Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相對大小如圖所示。圖中最穩定的點為( )A.A B.B C.C D.D 發布:2025/1/6 6:0:5組卷:0引用:1難度:0.9


