當前位置:
知識點挑題
請展開查看知識點列表
>
<
更多>>
 已完結
已完結
|
期末復習
典型試卷
考前必刷
瀏覽次數:862
更新:2025年06月03日
|
 已完結
已完結
|
熱點預測
高考復習
難題搶練
瀏覽次數:1145
更新:2025年05月26日
|
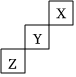 671.元素X、Y、Z在周期表中的相對位置如圖所示:已知Y元素原子的外圍電子排布為ns(n-1)np(n+1),則下列說法不正確的是( )
671.元素X、Y、Z在周期表中的相對位置如圖所示:已知Y元素原子的外圍電子排布為ns(n-1)np(n+1),則下列說法不正確的是( )A.Y元素原子的外圍電子排布為4s24p4 B.Y元素在周期表的第三周期第ⅥA族 C.X元素所在周期中所含非金屬元素最多 D.Z元素原子的核外電子排布式為1s22s22p63s23p63d104s24p3 發布:2024/12/30 17:0:2組卷:123引用:19難度:0.9672.下列對電子排布式或電子排布圖書寫的評價正確的是( )
選項 電子排布式或電子排布圖 評價 A. O原子的電子排布圖: 
錯誤;違反泡利不相容原理 B. N原子的電子排布圖: 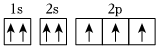
錯誤;違反洪特規則 C. Ca原子的電子排布式:1s22s22p63s23p63d2 錯誤;違反能量最低原理 D. Br-的電子排布式:[Ar]3d104s24p6 錯誤;違反能量最低原理 A.A B.B C.C D.D 發布:2024/12/30 17:0:2組卷:107引用:3難度:0.6673.通常情況下,微粒A和B為分子,C和E為陽離子,D為陰離子,它們都含有10個電子;B溶于A后所得的物質可電離出C和D;A、B、E三種微粒反應后可得C和一種白色沉淀.請回答.
(1)用化學符號表示下列微粒:C:,D:.
(2)寫出A、B、E三種微粒反應的離子方程式:.發布:2024/12/30 17:0:2組卷:48引用:19難度:0.5674.下列變化中釋放能量的是( )
A.1s22s22p63s1→1s22s22p6 B.N≡N(g)→N(g)+N(g) C.2px22py12pz1→2px12py12pz2 D.2H(g)→H-H(g) 發布:2024/12/30 17:0:2組卷:112引用:5難度:0.9675.下列關于σ鍵和π鍵的理解不正確的是( )
A.σ鍵一般能單獨形成,而π鍵一般不能單獨形成 B.σ鍵可以繞鍵軸旋轉,π鍵一定不能繞鍵軸旋轉 C.CH3-CH3.CH2=CH2.CH≡CH中σ鍵都是C-C鍵,所以鍵能都相同 D.碳碳雙鍵中有一個σ鍵,一個π鍵,碳碳三鍵中有一個σ鍵,兩個π鍵 發布:2024/12/30 17:0:2組卷:52引用:9難度:0.7676.下列粒子的半徑關系正確的是( )
A.r(Na)>r(Mg)>r(Al)>r(K) B.r(K +)>r(Ca 2+)>r(S 2-)>r(Cl -) C.r(Na)>r(K)>r(Ca)>r(Mg) D.r(F -)>r(Na +)>r(Mg 2+)>r(Al 3+) 發布:2024/12/30 17:0:2組卷:98引用:3難度:0.7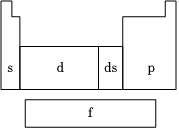 677.在研究原子核外電子排布與元素周期表的關系時,人們發現價電子排布相似的元素集中在一起,據此,人們將元素周期表分為五個區,并以最后填入電子的軌道能級符號作為該區的符號,如圖所示.
677.在研究原子核外電子排布與元素周期表的關系時,人們發現價電子排布相似的元素集中在一起,據此,人們將元素周期表分為五個區,并以最后填入電子的軌道能級符號作為該區的符號,如圖所示.
(1)在s區中,族序數最大、原子序數最小的元素原子的價電子的電子云形狀為;
(2)在d區中,族序數最大、原子序數最小的元素,常見離子的電子排布式為,其中較穩定的是;
(3)在ds區中,族序數最大、原子序數最小的元素,原子的價電子排布式為;
(4)在p區中,第二周期VA族元素原子的價電子排布圖為;
(5)在今常用于核能開發的元素是鈾和钚,它們在區中.發布:2024/12/30 17:0:2組卷:104引用:5難度:0.9678.根據原子核外電子排布規則,回答下列問題:
(1)寫出基態S原子的核外電子排布式,寫出基態24Cr原子的價電子排布式;
(2)寫出基態N的原子核外電子排布圖:。
(3)若將基態14Si的電子排布式寫成1s22s22p63s33p1,則它違背了;
(4)Fe3+比Fe2+的穩定性更(填“強”或“弱”),從結構上分析原因是。發布:2024/12/30 17:0:2組卷:50引用:4難度:0.5679.在d軌道中電子排布成
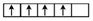 ,而不排布成
,而不排布成 ,其直接的依據是( )
,其直接的依據是( )A.能量最低原理 B.泡利原理 C.原子軌道能級圖 D.洪特規則 發布:2024/12/30 17:0:2組卷:76引用:3難度:0.8680.通常情況下,氯化鈉、氯化銫、二氧化碳和二氧化硅的晶體結構分別如圖所示:
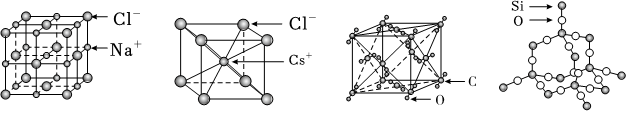
下列關于這些晶體結構和性質的敘述不正確的是( )A.同一主族的元素與另一相同元素所形成的化學式相似的物質不一定具有相同的晶體結構 B.在二氧化硅晶體中,平均每個Si原子形成4個Si-O共價單鍵 C.二氧化碳晶體是分子晶體,其中不僅存在分子間作用力,而且也存在共價鍵 D.氯化鈉、氯化銫和二氧化碳的晶體都有立方的晶胞結構,它們具有相似的物理性質 發布:2024/12/30 17:0:2組卷:85引用:5難度:0.8



