學習以下材料,回答(1)~(4)題。
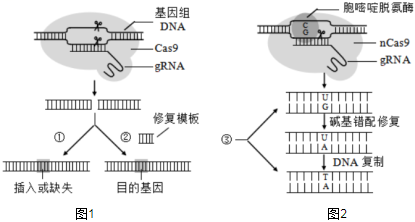
基因魔剪:CRISPR/Cas系統CRISPR/Cas基因編輯系統可對真核細胞的基因組進行特異編輯。CRISPR/Cas9系統由Cas9蛋白和人工設計的gRNA構成。在gRNA引導下,Cas9與靶序列結合并將DNA雙鏈切斷(通過設計gRNA中20個堿基的識別序列,可人為選擇DNA上的任一目標位點進行切割)。隨后細胞通過自身的DNA損傷修復機制,將斷裂上下游兩端的序列連接起來,但通常會在斷裂處造成少量核苷酸的插入或缺失。當DNA雙鏈斷裂后,如果細胞中有DNA修復模板(由需要插入的目的基因和靶序列上下游的同源序列組成),斷裂部分可依據修復模板進行精確修復,從而將目的基因插入到指定位點(圖1)。
科學家通過在Cas9基因中引入突變,獲得了只切割DNA一條鏈的nCas9,并將nCas9與胞嘧啶脫氨酶或腺嘌呤脫氨酶融合,開發出了單堿基編輯技術(圖2),能夠對靶位點進行精準的堿基編輯,最終可以分別實現C→T(G→A)或A→G(T→C)的堿基替換。對CRISPR/Cas系統改造后,還可用于激活或者抑制基因的轉錄等。
目前CRISPR/Cas9基因編輯技術存在一定的脫靶效應:正常情況下,gRNA通過20個核苷酸長度的引導序列與目標DNA序列發生堿基互補配對準確識別需要編輯的位點,然而有時會發生第18~20個堿基不匹配的情況,此時,Cas9可通過一個手指狀的結構緊緊抓住錯配區穩定住RNA-DNA雙鏈,從而為Cas9切割DNA鋪平道路,但這可能會導致Cas9在錯誤的基因位點切割雙鏈DNA,從而引發潛在風險。
盡管如此,CRISPR/Cas系統作為一種革命性的技術,其成本低、制作簡便、快捷高效等優點讓它迅速風靡于世界各地的實驗室,成為科研、醫療等領域的有效工具。
(1)利用CRISPR/Cas9系統進行基因編輯,需構建含gRNA基因和Cas9基因的 基因表達載體(或重組DNA分子、重組質粒)基因表達載體(或重組DNA分子、重組質粒),并導入受體細胞。Cas9蛋白與 限制限制酶的功能相似。gRNA依據 堿基互補配對堿基互補配對原則與靶序列特異性結合,引導Cas9蛋白進行切割。
(2)若用CRISPR/Cas9系統將某一基因從基因組序列中刪除,需要設計2個gRNA,使其分別與 靶基因兩端靶基因兩端的序列互補。有些遺傳病是由于基因中一個堿基對改變引起的,若要修正此基因突變,文中圖示的3種途徑中,③③(填“①”“②”或“③”)更為合適。
(3)研究者通過一些技術讓Cas9基因發生突變,使Cas9蛋白失去切割活性,可將CRISPR/Cas9用于抑制基因轉錄,實施的過程為:在gRNA的引導下,Cas9蛋白與靶基因的 啟動子啟動子結合,使 RNA聚合酶RNA聚合酶失去結合位點從而抑制靶基因的轉錄。
(4)請結合文章,提出降低CRISPR/Cas9系統脫靶效應的思路。設計gRNA的長度為17個堿基,避免第18~20個堿基不匹配時,導致錯誤位點的切割(或設計出特異性較強的gRNA,增強gRNA的特異性;通過設計Cas9,讓其手指狀結構遠離DNA序列,從而在gRNA與DNA錯配時,不會穩定錯配結構,避免在錯誤位點切割等)設計gRNA的長度為17個堿基,避免第18~20個堿基不匹配時,導致錯誤位點的切割(或設計出特異性較強的gRNA,增強gRNA的特異性;通過設計Cas9,讓其手指狀結構遠離DNA序列,從而在gRNA與DNA錯配時,不會穩定錯配結構,避免在錯誤位點切割等)。
【考點】基因工程在農牧、醫療、食品等方面的應用.
【答案】基因表達載體(或重組DNA分子、重組質粒);限制;堿基互補配對;靶基因兩端;③;啟動子;RNA聚合酶;設計gRNA的長度為17個堿基,避免第18~20個堿基不匹配時,導致錯誤位點的切割(或設計出特異性較強的gRNA,增強gRNA的特異性;通過設計Cas9,讓其手指狀結構遠離DNA序列,從而在gRNA與DNA錯配時,不會穩定錯配結構,避免在錯誤位點切割等)
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/14 8:0:9組卷:26引用:1難度:0.5
相似題
-
1.學習以下材料,回答(1)~(4)題。
利用抑制性tRNA進行無義突變遺傳病的治療
無義突變是由于某個堿基的改變使代表某種氨基酸的密碼子突變為終止密碼子(UAA、UAG或UGA),從而使肽鏈合成提前終止,造成蛋白質的功能改變,引發相關疾病。約有10%~15%的人類基因相關遺傳疾病是由無義突變引發的。常規的基因治療是將正常基因的cDNA序列或是有治療價值的基因(如CRISPR-Cas9相關的基因編輯工具)通過一定的方式導入人體靶細胞內,達到替代或修復缺陷基因、治療疾病的目的。導入基因插入位置不當、過高或過低表達,都可能會導致副作用。盡管基因編輯可以實現生理水平的基因表達,但基因編輯工具引入外源蛋白可能引發強烈的免疫反應仍然是巨大的挑戰。
抑制性tRNA(sup-tRNA)由天然tRNA改造而來,它的反密碼子通過堿基配對原則可以識別無義突變的終止密碼子,使得mRNA在翻譯至無義突變位點時不啟動翻譯終止而是繼續向后進行翻譯,獲得有功能的全長蛋白。
I型黏多糖貯積癥的病因,是相關基因發生無義突變,產生終止密碼子UAG。研究者構建小鼠該突變基因mldua和Flag基因融合的載體(圖1),以及針對該無義突變設計的sup-tRNA表達載體(產生的sup-tRNA能夠識別UAG并攜帶酪氨酸Tyr,簡寫作sup-tRNATyr),將其導入細胞進行研究,發現與具有相似作用的化合物G418比較,sup--tRNA的作用更加顯著(圖2);進一步利用重組腺相關病毒作為載體將sup-tRNA導入患病小鼠模型中,實驗顯示能夠降低黏多糖過度積存,實現對該病癥的有效治療,其療效可以持續半年以上。
從整體來看,G418在促進跨越無義突變位點繼續翻譯時引入的氨基酸較為隨機,而sup-tRNA引入的氨基酸較為單一,且不會影響內源tRNA穩態,所以sup-tRNA在個體治療中具有很高的安全性,因而在未來基因突變引起的疾病相關治療中具有非常大的應用前景。
(1)侵染時,作為載體的重組腺相關病毒與靶細胞膜上的發生識別,引發內吞,進入細胞后釋放單鏈DNA作為模板,利用宿主細胞的催化合成其互補DNA鏈,再經過過程產生sup-tRNA。
(2)除了引入的氨基酸較為單一,不影響內源tRNA穩態,我們還可推斷,用于治療的sup-tRNA在正常終止密碼子處(填“能”或“不能”)繼續往后翻譯,具有很高的安全性。
(3)研究者構建mldua突變基因和Flag基因融合的載體,目的是通過檢測來確定是否跨越無義突變位點繼續向后翻譯。實驗結果表明,相比于化合物G418,sup-tRNA在促進無義突變位點的翻譯方面更加有效,支持這一結論的依據是:。
(4)有文獻報道,已在近1000個不同的人類基因中發現了7500多個無義突變。常規的基因治療需要為每種疾病設計獨特的治療策略,這將是一項耗費驚人的項目。據此說明sup-tRNA的應用價值。發布:2025/1/3 8:0:1組卷:28引用:1難度:0.6 -
2.人類基因組計劃測定了人體的24條染色體,這24條染色體是( )
A.24對同源染色體的各一條 B.隨機抽取24條染色體 C.全部的常染色體 D.22對常染色體的各一條和X、Y染色體 發布:2024/12/31 0:30:1組卷:115引用:7難度:0.7 -
3.幾丁質是許多真菌細胞壁的重要成分,自然界有些植物能產生幾丁質酶催化幾丁質水解從而抵抗真菌感染。通過基因工程將幾丁質酶基因轉入沒有抗性的植物體內,可增強其抗真菌的能力。如圖表示為獲取幾丁質酶基因而建立cDNA文庫的過程。

(1)圖示以mRNA為材料通過法獲得cDNA,該方法依據的原理是,通過這種方法獲得的基因中因缺乏和結構,導致將其直接導入受體細胞中不能復制和表達。
(2)與選用老葉相比,選用嫩葉更容易提取到mRNA,原因是,且提取RNA時,提取液中需添加RNA酶抑制劑,其目的是。
(3)將從cDNA文庫中獲得的幾丁質酶基因和質粒載體用酶和DNA連接處理后連接起來,構建基因表達載體,DNA連接酶催化形成的化學鍵是。發布:2025/1/5 8:0:1組卷:5引用:1難度:0.7


