實驗室有一瓶敞口放置的氫氧化鈉固體,同學們對其是否變質以及變質情況進行探究。
【提出問題】敞口放置的氫氧化鈉固體是否變質呢?變質程度是怎樣的?
【猜想與假設】猜想Ⅰ:沒有變質;猜想Ⅱ:全部變質;猜想Ⅲ:部分變質。
【實驗探究】同學們分別設計了不同的方案進行探究,請你協助完成相關內容。
小芳設計的實驗方案如下:
| 實驗步驟 | 實驗現象 | 結論 |
| ①取少量固體樣品于試管中,加足量水溶解,滴加無色酚酞溶液 | (1) 溶液變紅色 溶液變紅色 |
猜想Ⅲ成立 |
| ②向步驟①的試管中滴加過量的稀鹽酸 | 有氣泡產生 |
(2)同學們討論認為:小芳的實驗結論不嚴密,理由是
完全變質后的碳酸鈉溶液顯堿性,也能使酚酞變紅色
完全變質后的碳酸鈉溶液顯堿性,也能使酚酞變紅色
。【拓展實驗】
(3)小華另取少量固體樣品溶于水,滴加足量的CaCl2溶液(顯中性),涉及的化學反應方程式為
Na2CO3+CaCl2═CaCO3↓+2NaCl
Na2CO3+CaCl2═CaCO3↓+2NaCl
。過濾后,對濾液 ①②④
①②④
(填序號),根據實驗現象,即可證明猜想Ⅲ成立。①測pH
②滴加MgSO4溶液
③加入稀鹽酸
④滴加CuCl2溶液
(4)為測定這瓶敞口放置的氫氧化鈉固體的純度,現取10.0g樣品于燒杯中,加水充分溶解,然后逐滴加入CaCl2溶液,反應過程中加入氯化鈣溶液的質量與生成沉淀的質量關系如圖甲所示(不考慮其他因素的影響),該樣品中氫氧化鈉的質量分數是
47%
47%
。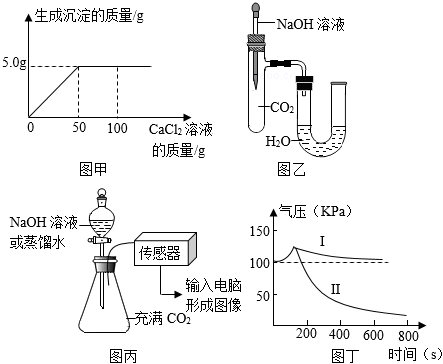
【學科融合】(5)按如圖乙所示裝置進行實驗。實驗前U型管兩端液面相平,將NaOH溶液滴入試管中,恢復到室溫后,U型管中的左端液面
上升
上升
。據此,小明同學得出“CO2與NaOH發生了化學反應”的結論。小紅認為小明結論證據不充足,理由是 二氧化碳能夠溶于水,也能夠導致左邊液面上升
二氧化碳能夠溶于水,也能夠導致左邊液面上升
。【再次實驗】(6)同學們用壓強傳感器研究水或等量NaOH溶液分別吸收CO2的效果,實驗裝置及測定結果如圖丙和圖丁所示。圖丁中
Ⅱ
Ⅱ
(填“Ⅰ”、“Ⅱ)表示等量NaOH溶液吸收CO2的曲線。【答案】溶液變紅色;完全變質后的碳酸鈉溶液顯堿性,也能使酚酞變紅色;Na2CO3+CaCl2═CaCO3↓+2NaCl;①②④;47%;上升;二氧化碳能夠溶于水,也能夠導致左邊液面上升;Ⅱ
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:78引用:4難度:0.5
相似題
-
1.實驗室有一瓶配制數天的Na2SO3溶液,現在對其成分進行檢測:
【成分猜想】猜想一:只有Na2SO3;
猜想二:;
猜想三:既有Na2SO3,也有Na2SO4。
【查閱資料】①Na2SO3易被空氣中的氧氣氧化生成Na2SO4.②BaSO4
不溶于稀鹽酸和稀硫酸。③Na2SO3和鹽酸、硫酸反應均生成SO2。
【方案設計】
【方案分析】方案 實驗操作 實驗現象 結論 一 
①加入足量的稀鹽酸
②再加入足量的BaCl2溶液
猜想三正確 二
①加入足 量的稀硫酸
量的稀硫酸
②再加入足量的BaCl2溶液有氣體和白色沉淀生成 猜想一或猜想三正確
(1)方案一中的實驗現象為;方案一中加入BaCl2溶液后發生反應的化學方程式為。
(2)方案二的設計是否合理:(填“合理”或“不合理”);若不合理。理由是。
【實驗結論】通過分析比較,方案設計(填“—”或“二”)合理。發布:2024/12/24 10:0:46組卷:350引用:3難度:0.5 -
2.氫氧化鈉變質的實驗探究:
I:向鈉離子質量分數均為2%的氯化鈉溶液、氫氧化鈉溶液、碳酸鈉溶液中滴加酚酞,氯化鈉溶液不變紅,氫氧化鈉溶液、碳酸鈉溶液變紅。
Ⅱ:一位實驗員在實驗室剛配制一定質量分數的氫氧化鈉溶液后,突然接到緊急任務離開,幾天后回到實驗室才發現沒有蓋上瓶塞。
(1)你認為能使酚酞變紅的微粒為。
A.Na+
B.OH-
C.或由CO2-3引發生成的OH-。CO2-3
(2)氫氧化鈉變質為碳酸鈉,反應的化學方程式為。溶液中的離子數量如何變化?。(填:不變、減少、增大)
(3)欲證明有氫氧化鈉變質為碳酸鈉,同學甲認為可選擇試劑a:稀鹽酸,同學乙認為可選擇試劑b;氯化鋇溶液,你的觀點是。(單項選擇題)
A.過量稀鹽酸
B.過量氯化鋇溶液
C.過量稀鹽酸和氯化鋇溶液均可以
D.過量稀鹽酸和氯化鋇溶液均不可以
(4)同學丙認為氫氧化鈉只有一部分變質為碳酸鈉,溶液中仍然含有氫氧化鈉,他通過設計以下實驗證明其結論是正確的。
第一步:取少量待測液,向其中加入過量的溶液,過濾;
第二步:向以上濾液中加入,出現的現象,則丙同學觀點正確。
(5)100g質量分數為A%的氫氧化鈉溶液有部分變質后,同學丁認為仍然可以通過設計實驗方案計算出A的數值,其具體的實驗方案如下:向變質后的溶液中加入過量的稀鹽酸,蒸發結晶,洗滌,干燥,得到5.85g固體,從而可以計算出A的數值。你認為是否可以?(填“可以”或“不可以”)。若不可以,請簡述理由,若可以,則寫出A的數值。發布:2024/12/25 15:0:2組卷:164引用:3難度:0.5 -
3.小強在實驗室里做實驗時,拿出一瓶久置的氫氧化鈣粉末,進行如下實驗:
(1)取氫氧化鈣粉末溶于足量水中,有現象出現,小強判斷該藥品已變質。并寫出氫氧化鈣變質的反應方程式。
(2)小強進一步做如下實驗探究,請你參與并完成表:實驗操作步驟 實驗現象 實驗結論 取樣、加適量的水,攪拌,過濾。 ①取少量濾渣于試管中,加入少量的 。粉末變質。 ②取少量濾液于試管中,滴入少量的 溶液。氫氧化鈣粉末部分變質。 發布:2024/11/27 8:0:1組卷:108引用:1難度:0.5


