通過半學期的化學學習,我們一起利用學過的知識完成以下實驗的探究吧!
(1)【實驗一】
①利用紅磷燃燒測定空氣里氧氣含量的實驗如圖所示,反應的化學方程式為 4P+5O2 點燃 2P2O54P+5O2 點燃 2P2O5,該反應屬于 化合反應化合反應(填基本反應類型)。

②用四硫化鈉(Na2S4)固體可替代紅磷測定空氣中氧氣的體積分數。反應原理為2Na2S4+O2+2H2O═8S↓+4NaOH(氫氧化鈉),小資料:四硫化鈉(Na2S4)與氧氣、水反應生成難溶于水的固體硫(S)和易溶于水的氫氧化鈉。
(實驗過程)
①取足量的四硫化鈉固體加入試管中,再加入適量的水,迅速塞緊橡膠塞,充分振蕩。測量液面至橡膠塞下沿的距離,記錄數據h1(如圖1所示)。
②將該試管插入水中(如圖2所示),拔下橡膠塞,觀察到試管內液面上升,至液面度不再改變時,塞緊橡膠塞,將試管取出,倒轉過來,測量液面至橡膠塞下沿的距離記錄數據h2。理論上h1:h2=100:79100:79。

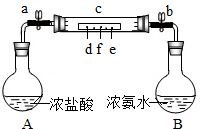
(2)【實驗二】資料①:濃鹽酸易揮發出氯化氫氣體,濃氨水易揮發出氨氣(NH3),氨氣與氯化氫氣體相遇會產生大量白煙,這是因為兩者發生反應生成了氯化銨固體;
資料②:氣體的相對分子質量越小,其分子的運動速率越快。
如圖所示,燒瓶A中盛有濃鹽酸,燒瓶B中盛有濃氨水,在長玻璃管外壁上用記號筆做了d、e、f三個標記,請回答下列問題:
 ①寫出氯化銨的化學式為 NH4ClNH4Cl。
①寫出氯化銨的化學式為 NH4ClNH4Cl。
②實驗開始時打開開關a、b,一會兒后玻璃管中產生大量白煙,此現象能說明分子具有的性質是 分子是不斷運動的分子是不斷運動的。
③你認為玻璃管中白煙最濃厚的地方是 dd(選填“d”“e”或“f”)。
(3)【實驗三】為了研究質量守恒定律,設計了如圖“白磷燃燒前后質量測定”的實驗,請分析有關問題:
 ①燃燒前:錐形瓶的底部鋪有一層細沙,燃燒前稱量,錐形瓶的總質量為27.2g,則圖中托盤天平中游碼的讀數為 2.22.2g。
①燃燒前:錐形瓶的底部鋪有一層細沙,燃燒前稱量,錐形瓶的總質量為27.2g,則圖中托盤天平中游碼的讀數為 2.22.2g。
②白磷燃燒:白磷燃燒過程中看到的現象是 產生白煙,放熱產生白煙,放熱。
③燃燒后稱量:發現托盤天平指針偏向右邊,造成的原因可能 沒有冷卻至室溫,氣球膨脹導致浮力增大沒有冷卻至室溫,氣球膨脹導致浮力增大(寫一條原因即可)。
點燃
點燃
【答案】4P+5O2 2P2O5;化合反應;100:79;NH4Cl;分子是不斷運動的;d;2.2;產生白煙,放熱;沒有冷卻至室溫,氣球膨脹導致浮力增大
點燃
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:28引用:1難度:0.5
相似題
-
1.化學符號是學習化學的重要工具。下列說法正確的是( )
A.KClO3,KCl中鉀元素的化合價不相同 B. 
二者組成的化合物是由離子構成C. 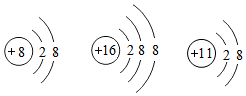
表示的粒子都是陰離子D.MnO2+4HCl(濃) MnCl2+2X+Cl2↑,其中X的化學式是H2O2△發布:2025/1/2 8:30:5組卷:32引用:2難度:0.5 -
2.咸寧城際鐵路的建成將進一步推動我市經濟的發展,在修建鐵路的土石方爆破中要用到黑火藥,黑火藥爆炸時發生反應的化學方程式是2KNO3+3C+S
K2S+3CO2↑+X↑,根據以上信息,下列說法錯誤的是( )點燃A.X的化學式是N2 B.黑火藥在混合物 C.KNO3中氮元素的化合價為+5價 D.KNO3屬于氨肥 發布:2024/12/29 16:0:4組卷:287引用:43難度:0.9 -
3.某種家用的消毒液的主要成分是次氯酸鈉(NaClO),制取NaClO的化學方程式為:Cl2+2NaOH=NaClO+NaCl+X,下列說法錯誤的是( )
A.X的化學式為H2O B.反應中用到的NaOH俗稱純堿 C.該化學方程式中涉及到兩種鹽 D.反應前后氯元素化合價既升高又降低 發布:2025/1/3 8:0:1組卷:17引用:1難度:0.8


