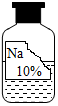
 實(shí)驗(yàn)室有一瓶標(biāo)簽殘缺并且瓶蓋沒有完全密封的無色溶液(如圖),化學(xué)小組的同學(xué)經(jīng)過詢問老師后只知道是氯化鈉、氫氧化鈉、碳酸鈉、碳酸氫鈉中的一種溶液,為確認(rèn)原瓶中是何種溶質(zhì),化學(xué)小組的同學(xué)進(jìn)行了如下的探究活動:
實(shí)驗(yàn)室有一瓶標(biāo)簽殘缺并且瓶蓋沒有完全密封的無色溶液(如圖),化學(xué)小組的同學(xué)經(jīng)過詢問老師后只知道是氯化鈉、氫氧化鈉、碳酸鈉、碳酸氫鈉中的一種溶液,為確認(rèn)原瓶中是何種溶質(zhì),化學(xué)小組的同學(xué)進(jìn)行了如下的探究活動:
【探究一】
甲同學(xué)用玻璃棒蘸取瓶中溶液至pH試紙上,與標(biāo)準(zhǔn)比色卡比較,測得pH=12;乙同學(xué)提出先查閱常溫下有關(guān)物質(zhì)的溶解度信息(如表):
| 物質(zhì) | 氯化鈉 | 氫氧化鈉 | 碳酸鈉 | 碳酸氫鈉 |
| 常溫下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
(1)從甲同學(xué)的實(shí)驗(yàn)結(jié)果判斷:可知原溶液的溶質(zhì)一定不是
NaCl
NaCl
(填化學(xué)式)。(2)從乙同學(xué)查閱到的溶解度信息判斷,原溶液的溶質(zhì)一定不是
NaHCO3
NaHCO3
(填化學(xué)式)。【探究二】
丙同學(xué)在甲、乙兩同學(xué)探究結(jié)果的基礎(chǔ)上進(jìn)一步進(jìn)行實(shí)驗(yàn):取少量瓶中溶液于試管中,加入過量的稀鹽酸,觀察到
有氣泡產(chǎn)生
有氣泡產(chǎn)生
(填實(shí)驗(yàn)現(xiàn)象),由此丙同學(xué)得出結(jié)論:原溶液的溶質(zhì)為碳酸鈉溶液。但其他同學(xué)認(rèn)為丙同學(xué)的結(jié)論不一定可靠。同學(xué)們經(jīng)過積極思考并討論后,繼續(xù)實(shí)驗(yàn):【探究三】
| 步驟 | 實(shí)驗(yàn)操作 | 實(shí)驗(yàn)現(xiàn)象 |
| 1 | 取少量原瓶中溶液至試管,滴加足量氯化鈣溶液 | 產(chǎn)生白色沉淀 |
| 2 | 靜置后,取少量上層清液,向其中滴加硫酸銅溶液 | 無明顯現(xiàn)象 |
【探究四】
取8.4g瓶中溶液,加入氯化鈣溶液至恰好完全反應(yīng),過濾,將濾渣洗滌、干燥后稱量,測得沉淀質(zhì)量為1.0g。請你計(jì)算:當(dāng)前該瓶溶液中溶質(zhì)的質(zhì)量分?jǐn)?shù)為
12.6%
12.6%
(精確到0.1%)。【實(shí)驗(yàn)結(jié)論】該試劑瓶上原標(biāo)簽的內(nèi)容為“
NaOH10%(或NaOH溶液10%)
NaOH10%(或NaOH溶液10%)
”,理由是 當(dāng)前瓶中溶液為溶質(zhì)質(zhì)量分?jǐn)?shù)為12.6%的Na2CO3溶液,與原標(biāo)簽溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)10%相比明顯增大(合理描述均可)
當(dāng)前瓶中溶液為溶質(zhì)質(zhì)量分?jǐn)?shù)為12.6%的Na2CO3溶液,與原標(biāo)簽溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)10%相比明顯增大(合理描述均可)
。【討論與交流】老師指出【探究三】中所得結(jié)論仍然不一定可靠的理由是
該Na2CO3溶液可能是由NaOH溶液完全變質(zhì)形成
該Na2CO3溶液可能是由NaOH溶液完全變質(zhì)形成
。【考點(diǎn)】缺失標(biāo)簽的藥品成分的探究;鹽的化學(xué)性質(zhì).
【答案】NaCl;NaHCO3;有氣泡產(chǎn)生;12.6%;NaOH10%(或NaOH溶液10%);當(dāng)前瓶中溶液為溶質(zhì)質(zhì)量分?jǐn)?shù)為12.6%的Na2CO3溶液,與原標(biāo)簽溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)10%相比明顯增大(合理描述均可);該Na2CO3溶液可能是由NaOH溶液完全變質(zhì)形成
【解答】
【點(diǎn)評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:152引用:4難度:0.4
相似題
-
 1.某化學(xué)興趣小組的同學(xué)在整理化學(xué)藥品柜時(shí)【提出問題】這瓶無色溶液是什么物質(zhì)的溶液?
1.某化學(xué)興趣小組的同學(xué)在整理化學(xué)藥品柜時(shí)【提出問題】這瓶無色溶液是什么物質(zhì)的溶液?
【查閱資料】①20℃是碳酸鈉的溶解度是21.8g,碳酸氫鈉的溶解度是9.6g,硫酸鈉的溶解度19.5g,硝酸鈉的溶解度是88g。
②碳酸鋇是不溶于水的白色固體,硫酸鋇是既不溶解于水又不溶解于酸的白色固體;
③Ca(OH)2和Ba(OH)2的不同溫度下的溶解度如表所示:
【猜想與假設(shè)】小組同學(xué)提出了如下假設(shè):溫度(℃) 10 20 30 40 50 60 Ca(OH)2 0.17g 0.16g 0.15g 0.14g 0.13g 0.12g Ba(OH)2 2.48g 3.89g 5.59g 8.22g 13.12g 20.94g
①碳酸鈉溶液;②硫酸鈉溶液;③碳酸氫鈉溶液;④硝酸鈉溶液
【討論交流】在老師的指導(dǎo)下,小組同學(xué)認(rèn)為假設(shè)不合理,理由是。
【進(jìn)行實(shí)驗(yàn)】小組同學(xué)設(shè)計(jì)并進(jìn)行了如下實(shí)驗(yàn),請你完善小組同學(xué)的“相互評價(jià)”。
【實(shí)驗(yàn)反思】請寫出硫酸鈉和氫氧化鋇反應(yīng)的化學(xué)方程式實(shí)驗(yàn)組別 操作、現(xiàn)象與結(jié)論 結(jié)論與評價(jià) 第一組 取少量的樣品溶液于一試管中,向其中加入稀鹽酸,試管中無明顯現(xiàn)象。猜想②成立。 你認(rèn)為此結(jié)論 (填“正確”或不正確”),理由是。第二組 取少量的樣品溶液于一試管中,向其中加入氫氧化鋇溶液,試管中出現(xiàn)白色沉淀。猜想②成立。 此結(jié)論不正確,要想進(jìn)一步確定猜想②成立,還需進(jìn)行的實(shí)驗(yàn)是 。。
【注意:若答對下列兩個(gè)小題獎(jiǎng)勵(lì)4分,化學(xué)試卷總分不超過60分】
【拓展提升】長期存放的氫氧化鈉溶液會變質(zhì)生成碳酸鈉,為探究氫氧化鈉變質(zhì)的程度,實(shí)驗(yàn)室常用先加過量的氯化鈣溶液或氯化鋇溶液充分反應(yīng)后過濾,再在濾液中滴加酚酞溶液的方案進(jìn)行實(shí)驗(yàn)。
【實(shí)驗(yàn)反思】實(shí)驗(yàn)發(fā)現(xiàn)加氯化鋇溶液比加氯化鈣溶液實(shí)驗(yàn)結(jié)果更準(zhǔn)確,原因是。如果使用氯化鈣溶液,要達(dá)到實(shí)驗(yàn)?zāi)康模阏J(rèn)為改進(jìn)實(shí)驗(yàn)的方法是。發(fā)布:2024/12/25 16:30:1組卷:91引用:2難度:0.5 -
2.倉庫中有一包氮肥的包裝標(biāo)簽?zāi):磺澹型瑢W(xué)進(jìn)行了以下探究:
(1)操作③用玻璃棒攪拌的目的是.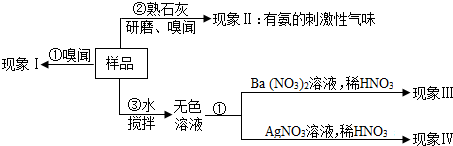
(2)請完成如表(已知AgCl和BaSO4是難溶于水和酸的白色固體):
(3)若現(xiàn)象Ⅲ、Ⅳ都無現(xiàn)象,則該氮肥可能是假設(shè)和現(xiàn)象 判斷和化學(xué)方程式 a 若現(xiàn)象I為無氨味. 則樣品中不含 (填名稱).b 由操作②現(xiàn)象判斷. 該樣品一定含有 離子.c 若現(xiàn)象Ⅲ為白色沉淀,現(xiàn)象Ⅳ為無沉淀. 則樣品中含有 (寫名稱),該反應(yīng)的化學(xué)方程式為.d 若現(xiàn)象Ⅲ為“無沉淀”,現(xiàn)象Ⅳ為白色沉淀. 則樣品中含有 (寫化學(xué)式),該反應(yīng)的化學(xué)方程式為.(寫化學(xué)式);若操作②現(xiàn)象為無氣味、現(xiàn)象Ⅲ、Ⅳ無現(xiàn)象,則該氮肥可能是(只寫一種).發(fā)布:2024/12/24 11:1:11組卷:356引用:5難度:0.1 -
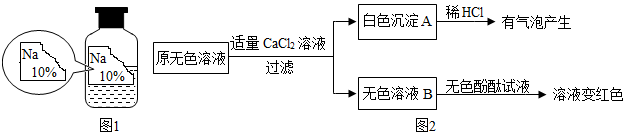
3.實(shí)驗(yàn)室有一瓶標(biāo)簽殘缺并且瓶蓋沒有完全密封的無色溶液(如圖1),化學(xué)小組的同學(xué)經(jīng)過詢問老師后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一種溶液,為確認(rèn)原瓶中是何種溶質(zhì)并判斷其是否變質(zhì),化學(xué)小組的同學(xué)進(jìn)行了如下的探究活動:
【進(jìn)行猜想】
猜想I:原溶液的溶質(zhì)是NaCl;
猜想Ⅱ:原溶液的溶質(zhì)是NaOH;
猜想Ⅲ:原溶液的溶質(zhì)是Na2CO3;
猜想 IV:原溶液的溶質(zhì)是NaHCO3。
【查閱資料】常溫下,有關(guān)物質(zhì)的相關(guān)信息如表:
從物質(zhì)的相關(guān)信息可知,原溶液的溶質(zhì)一定不是NaHCO3,因?yàn)?物質(zhì) NaCl NaOH Na2CO3 NaHCO3 常溫下的溶解度/g 36 109 21.5 9.6 常溫下稀溶液的pH 7 13 11 9 。
【進(jìn)行實(shí)驗(yàn)】
(1)取少量樣品,測得溶液的pH大于7,則原溶液的溶質(zhì)肯定不是。
(2)同學(xué)們另取樣品又進(jìn)行了如下實(shí)驗(yàn),實(shí)驗(yàn)過程如圖2:
①生成白色沉淀A的化學(xué)方程式。
②通過實(shí)驗(yàn)可以判斷樣品無色溶液中含有的溶質(zhì)有
【獲得結(jié)論】
實(shí)驗(yàn)完成后,最終得到的結(jié)論:原瓶中的溶質(zhì)是,且已變質(zhì)。發(fā)布:2024/12/25 16:0:1組卷:142引用:5難度:0.5


