某化學興趣小組的同學設計了如圖1所示的裝置,用紅磷燃燒來測定空氣中氧氣的含量。
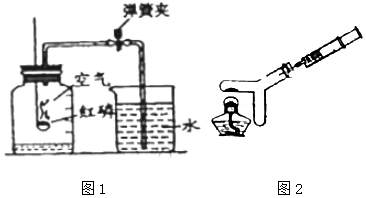
(1)若實驗成功,紅磷熄滅后,冷卻到室溫,打開彈簧夾水能倒吸入集氣瓶的原因是 磷燃燒消耗了氧氣,裝置中壓強減小磷燃燒消耗了氧氣,裝置中壓強減小。
(2)集氣瓶中剩余的氣體主要是 氮氣氮氣,本實驗可推知剩余氣體的化學性質有(寫一點):不燃燒也不支持燃燒不燃燒也不支持燃燒。
(3)在該實驗中不能用硫代替紅磷,主要原因是 硫燃燒生成二氧化硫氣體,裝置中壓強幾乎不變,水不能進入裝置硫燃燒生成二氧化硫氣體,裝置中壓強幾乎不變,水不能進入裝置。
(4)為了提高實驗的準確性,上述實驗應注意的事項是 等裝置冷卻至室溫后才能打開止水夾(合理即可)等裝置冷卻至室溫后才能打開止水夾(合理即可)(寫一點)。
(5)該化學興趣小組的同學在完成了上述課本上的“空氣中氧氣的含量測定”的實驗之后,認為課本實驗存在不足,興趣小組同學在教師的指導下將原裝置改進如圖2所示,成功的測出空氣中氧氣的含量。以下是他們的探究過程:
已知:Y型管體積(已去除膠塞占的體積)為amL,注射器中水的體積為bmL。
實驗步驟:檢查氣密性;用酒精燈加熱紅磷至燃燒;反應結束并冷卻后,讀取注射器中水體積為cmL。
①實驗中紅磷要足量,目的是 保證氧氣完全被消耗保證氧氣完全被消耗。
②根據實驗數據,求算空氣中氧氣體積分數的計算式為 bmL-cmLamL×100%bmL-cmLamL×100%。
③請結合上面的課本裝置圖分析,該改進裝置比課本裝置有哪些優點:(回答一點即) 實驗更環保且讀數更準確實驗更環保且讀數更準確。
bm
L
-
cm
L
am
L
×
100
%
bm
L
-
cm
L
am
L
×
100
%
【考點】空氣組成的測定.
【答案】磷燃燒消耗了氧氣,裝置中壓強減小;氮氣;不燃燒也不支持燃燒;硫燃燒生成二氧化硫氣體,裝置中壓強幾乎不變,水不能進入裝置;等裝置冷卻至室溫后才能打開止水夾(合理即可);保證氧氣完全被消耗;;實驗更環保且讀數更準確
bm
L
-
cm
L
am
L
×
100
%
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:11引用:1難度:0.6
相似題
-
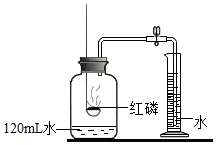 1.用氣密性良好的裝置測定空氣中氧氣的含量。
1.用氣密性良好的裝置測定空氣中氧氣的含量。
(1)紅磷燃燒的化學方程式是。
(2)若使用500mL的集氣瓶,圖中量筒的規格應是(填序號)。
A.20mL
B.50mL
C.100mL
(3)實驗結束后,測得氧氣的體積分數偏小。產生此結果的原因可能是(答1條即可)。發布:2024/12/24 9:30:1組卷:35引用:2難度:0.6 -
2.用如圖裝置測定空氣中氧氣的含量,物質M應該選用( )
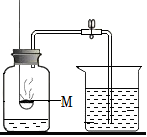
A.鐵片 B.蠟燭 C.木炭 D.紅磷 發布:2024/12/25 12:30:1組卷:10引用:2難度:0.6 -
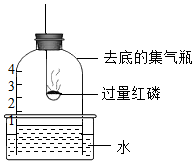 3.用如圖所示裝置進行實驗。下列現象能證明空氣中O2含量的是( )
3.用如圖所示裝置進行實驗。下列現象能證明空氣中O2含量的是( )A.水槽中液面下降 B.紅磷燃燒,產生白煙 C.瓶中液面先下降,后上升 D.瓶中液面最終上升至1處 發布:2024/12/25 13:0:1組卷:241引用:3難度:0.6


