實驗室常用溴化鈉,濃硫酸與乙醇共熱來制取溴乙烷,其反應的化學方程式如下:
NaBr+H2SO4═NaHSO4+HBr C2H5OH+HBr△C2H5Br+H2O
試回答下列各問:
(1)第二步反應實際上是一個可逆反應,在實驗中可采取增大某種反應物的量,如加過量NaBr以增加HBr的量增大某種反應物的量,如加過量NaBr以增加HBr的量和減小某種生成物的量,以使平衡正向移動,如加過量濃H2SO4吸水減小某種生成物的量,以使平衡正向移動,如加過量濃H2SO4吸水的措施,以提高溴乙烷的產率.
(2)濃H2SO4在實驗中的作用是在第一個反應中是反應物,在第二個反應中是吸水劑在第一個反應中是反應物,在第二個反應中是吸水劑,其用量(物質的量)應大于大于NaBr的用量(填大于、等于或小于).
(3)實驗中可能發生的有機副反應(用化學方程式表示)是2C2H5OH140℃濃硫酸C2H5OC2H5+H2O2C2H5OH140℃濃硫酸C2H5OC2H5+H2O和C2H5OH170℃濃硫酸C2H4↑+H2OC2H5OH170℃濃硫酸C2H4↑+H2O.
△
140
℃
濃硫酸
140
℃
濃硫酸
170
℃
濃硫酸
170
℃
濃硫酸
【考點】溴乙烷的制取.
【答案】增大某種反應物的量,如加過量NaBr以增加HBr的量;減小某種生成物的量,以使平衡正向移動,如加過量濃H2SO4吸水;在第一個反應中是反應物,在第二個反應中是吸水劑;大于;2C2H5OHC2H5OC2H5+H2O;C2H5OHC2H4↑+H2O
140
℃
濃硫酸
170
℃
濃硫酸
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/5/27 14:0:0組卷:62引用:1難度:0.5
相似題
-
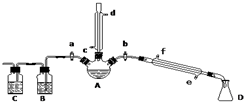 1.某興趣小組在實驗室用加熱乙醇、濃H2SO4、溴化鈉和少量水的混合物來制備溴乙烷,并檢驗反應的部分副產物.設計了如圖裝置,其中夾持儀器、加熱儀器及冷卻水管沒有畫出.請根據實驗步驟回答:
1.某興趣小組在實驗室用加熱乙醇、濃H2SO4、溴化鈉和少量水的混合物來制備溴乙烷,并檢驗反應的部分副產物.設計了如圖裝置,其中夾持儀器、加熱儀器及冷卻水管沒有畫出.請根據實驗步驟回答:
(1)儀器A的名稱是,儀器A正上方冷凝管冷凝水從口進入,儀器A右方冷凝管冷凝水從口進入;
(2)制備操作中,加入的少量的水,其目的是(填字母);
a.減少副產物烯和醚的生成 b.減少Br2的生成
c.減少HBr的揮發 d.水是反應的催化劑
(3)加熱片刻后,A中的混合物出現橙紅色,該橙紅色物質可能是;
(4)理論上上述反應的副產物還可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氫等
①檢驗副產物中是否含有溴化氫:熄滅酒精燈,在豎直冷凝管上方塞上塞子、打開a,利用余熱繼續反應直至冷卻,通過B、C裝置檢驗.B、C中應盛放的試劑分別是、;
②檢驗副產物中是否含有乙醚:通過紅外光譜儀鑒定所得產物中含有“-CH2CH3”基團,來確定副產物中存在乙醚.你認為對該同學的觀點;(填“正確”或“不正確”),原因是.發布:2024/12/21 8:0:2組卷:93引用:1難度:0.1 -
2.實驗室用如圖所示的裝置制取溴乙烷。在試管Ⅰ中依次加入2mL蒸餾水、4mL濃硫酸、2mL95%的乙醇和3g溴化鈉粉末,在試管Ⅱ中加入冰水混合物,在燒杯中注入自來水。加熱試管Ⅰ至微沸狀態數分鐘后,冷卻。

(1)試管Ⅰ中濃硫酸與溴化鈉加熱反應生成氫溴酸,寫出氫溴酸與乙醇在加熱時反應的化學方程式。
(2)溴乙烷為無色油狀液體,其官能團為(寫名稱)。
(3)若試管Ⅱ中獲得的有機物呈棕黃色,除去其中的雜質最佳的試劑是(填序號)。
A.CCl4
B.NaOH溶液
C.Na2SO3溶液
D.稀硫酸
(4)設計實驗證明溴乙烷中含有溴元素(說明操作、現象和結論)。
(5)已知溴乙烷可以與鈉發生反應:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr。應用該反應原理,下列化合物中可以與鈉反應合成環丁烷的是(填序號)。
A.CH3CH2CH2CHBr
B.CH3CHBrCH2CH2Br
C.CH3CH2CHBrCH2Br
D.CH2BrCH2CH2CH2Br
(6)寫出由溴苯( )制備環己酮(
)制備環己酮( )的流程。 。發布:2024/9/20 2:0:8組卷:53引用:1難度:0.6
)的流程。 。發布:2024/9/20 2:0:8組卷:53引用:1難度:0.6 -
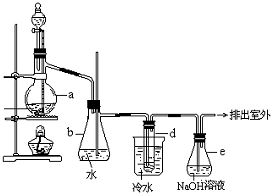 3.醇與氫鹵酸反應是制備鹵代烴的重要方法.實驗室制備溴乙烷的裝置如圖所示,其中錐形瓶b是安全瓶,試管d中裝有少量蒸餾水.已知溴乙烷的沸點為38.4℃,密度為1.43g/mL;
3.醇與氫鹵酸反應是制備鹵代烴的重要方法.實驗室制備溴乙烷的裝置如圖所示,其中錐形瓶b是安全瓶,試管d中裝有少量蒸餾水.已知溴乙烷的沸點為38.4℃,密度為1.43g/mL;
(1)制備溴乙烷需要用到蒸餾水、乙醇、溴化鈉、濃硫酸,在燒瓶中加入這幾種物質的順序依次是.
(2)小火加熱,在燒瓶中發生的主要反應有①;
②.
(3)冷水的作用;d試管中的現象.
(4)用這種方法制取的溴乙烷中的含少量雜質Br2,欲除去溴代烷中的少量雜質Br2,下列供選試劑中最適合的是.
A.NaI溶液 B.NaOH溶液 C.Na2SO3溶液 D.KCl溶液
(5)容器e中NaOH溶液的作用是.發布:2024/11/16 8:0:2組卷:148引用:3難度:0.1


