種類繁多的金屬材料已成為社會發展的重要物質基礎。
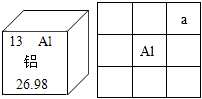
(1)如圖是鋁在元素周期表中的信息,則a元素的名稱是 碳碳。
(2)北京冬奧會國家速滑館“冰絲帶”采用單層雙向正交馬鞍形索網鋼結構,和純鐵相比,呈現了鋼的優點 硬度大硬度大(寫出一條即可)。
(3)鐵生銹是生活中常見的現象,實際上是鐵與空氣中的 氧氣和水氧氣和水同時發生化學反應的過程。通常可用除銹劑(含有鹽酸)除去鐵銹(Fe2O3),寫出該反應的化學方程式 Fe2O3+6HCl=2FeCl3+3H2OFe2O3+6HCl=2FeCl3+3H2O。
(4)已知由一氧化碳發生裝置得到的CO中混有雜質CO2和H2O。實驗室按照如圖所示裝置制取純凈、干燥的CO,然后用CO還原Fe2O3,并檢驗氣體產物。
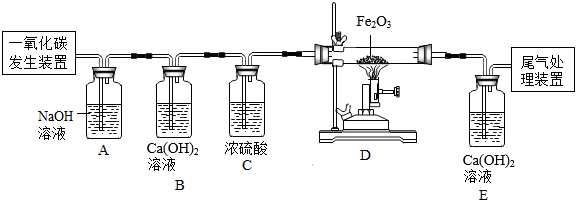
①B裝置的作用是 檢驗二氧化碳是否被吸收完檢驗二氧化碳是否被吸收完。
②寫出D裝置中反應的化學方程式 3CO+Fe2O3 高溫 2Fe+3CO23CO+Fe2O3 高溫 2Fe+3CO2。
③請設計實驗檢驗A溶液中的溶質,取反應后的溶液少許,向其中加入過量氯化鈣溶液,待沉淀完全后,取上層清液,滴入幾滴無色酚酞溶液,若溶液變紅色,說明溶質是氫氧化鈉和碳酸鈉,若溶液不變色,說明溶質只有碳酸鈉取反應后的溶液少許,向其中加入過量氯化鈣溶液,待沉淀完全后,取上層清液,滴入幾滴無色酚酞溶液,若溶液變紅色,說明溶質是氫氧化鈉和碳酸鈉,若溶液不變色,說明溶質只有碳酸鈉(簡要寫出實驗步驟、現象及結論)。
(5)近年來,我國工業利用“鋁熱反應”焊接鋼軌、冶煉難熔金屬等,其原理是在高溫下用鋁將某些金屬從其氧化物中置換出來。現有10.8t的鋁與四氧化三鐵反應來制取鐵,理論上可以制取鐵的質量是多少?
高溫
高溫
【答案】碳;硬度大;氧氣和水;Fe2O3+6HCl=2FeCl3+3H2O;檢驗二氧化碳是否被吸收完;3CO+Fe2O3 2Fe+3CO2;取反應后的溶液少許,向其中加入過量氯化鈣溶液,待沉淀完全后,取上層清液,滴入幾滴無色酚酞溶液,若溶液變紅色,說明溶質是氫氧化鈉和碳酸鈉,若溶液不變色,說明溶質只有碳酸鈉
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:23引用:3難度:0.4
相似題
-
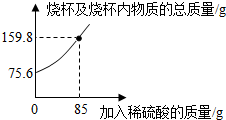 1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
1.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為52.2g的燒杯中,然后緩慢加入一定質量的稀硫酸,當加稀硫酸質量為85g時,反應恰好完全(雜質不反應且產生的氣體全部逸出),反應過程中的質量關系如圖.完成下列問題:
(1)該實驗取用的樣品質量為g.
(2)計算樣品中鐵的質量分數(寫出解題過程).發布:2025/1/9 8:0:2組卷:139引用:39難度:0.1 -
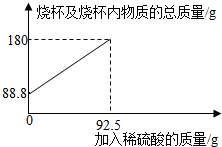 2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
2.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入92.5g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了10g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:4引用:1難度:0.3 -
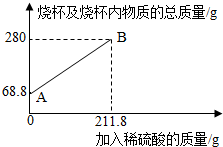 3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
3.為測定某碳素鋼樣品中鐵的質量分數,現取一定質量的樣品粉末于質量為51.8克的燒杯中,然后逐步加入一定質量分數的稀硫酸,當加入211.8g稀硫酸時恰好完全反應,加入稀硫酸的質量與燒杯及燒杯內物質的總質量的關系如圖。
(1)該實驗取用的樣品質量為g。
(2)求樣品中鐵的質量分數;反應后所得溶液中的溶質的質量分數。(寫出計算過程,結果保留一位小數)
(3)反應結束后,小明不慎向燒杯中多加了20g稀硫酸,若在圖中補繪此過程中稀硫酸的質量與燒杯及燒杯內物質的總質量的關系圖,所得線段的終點位于線段AB延長線的(填:上方、下方或線上)。發布:2025/1/9 8:0:2組卷:8引用:1難度:0.3


