含碳物質的中學化學研究的重要內容.
(1)“低碳生活”倡導低能量、低消耗,主要是為了減少CO2CO2(填化學式)的排放量.
(2)圖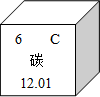 為元素周期表中的一格,下列說法不正確的是CC(填標號)
為元素周期表中的一格,下列說法不正確的是CC(填標號)
A.碳元素屬于非金屬元素 B.碳原子核內質子數為6
C.碳元素的原子結構示意圖為圖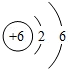 D.碳的相對原子質量是12.01
D.碳的相對原子質量是12.01
(3)為探究一瓶氫氧化鈉固體的變質情況,同學們進行了如下實驗.
①取少量該固體樣品置于試管中,向其中加入一種無色溶液,發現有氣泡產生,說明該樣品中含有碳酸鈉碳酸鈉,由此可確定該固體已發生變質,則無色溶液可能是鹽酸鹽酸.
②為探究該固體中是否還有未變質的氫氧化鈉,同學們又進行了如下表所示的實驗.已知碳酸鈉的水溶液呈堿性,它的存在會對氫氧化鈉的檢驗造成干擾.請根據部分物質的溶解性表(20℃)所提供的信息,將表填寫完整.
| 陰離子 陽離子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、揮 | 溶、揮 | 溶 | 溶、揮 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 實驗目的 | 實驗操作 | 現象 | 結論或化學方程式 |
| 除去碳酸鈉 | 取少量該固體樣品溶 于水配成溶液,滴加適量的 氯化鋇溶液 氯化鋇溶液 溶液,充分反應后過濾 | 有白色沉淀生成 | 有關反應的化學方程式為 Na2CO3+BaCl2═BaCO3↓+2NaCl Na2CO3+BaCl2═BaCO3↓+2NaCl |
| 檢驗是否含有 氫氧化鈉 | 在濾液中滴加酚酞溶液 | 溶液變紅色 溶液變紅色 | 該樣品中含有氫氧化鈉 |
【答案】CO2;C;碳酸鈉;鹽酸;氯化鋇溶液;Na2CO3+BaCl2═BaCO3↓+2NaCl;溶液變紅色
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:24引用:2難度:0.1
相似題
-
1.下列關于碳及其化合物說法正確的是( )
A.金剛石、石墨物理性質差異大,是由于構成它們的原子內部結構不同 B.一氧化碳中的雜質二氧化碳,可通過灼熱的氧化銅粉末除去 C.強調低碳生活,是因為二氧化碳有毒 D.金剛石和C60都由原子構成 發布:2024/12/25 13:30:1組卷:71引用:2難度:0.9 -
2.中國政府承諾“努力爭取2060年前實現碳中和”,“碳中和”是使碳排放與碳吸收達平衡,實現二氧化碳相對“零排放”。為了實現碳中和,從實際出發,下列說法錯誤的是( )
A.露天焚燒農作物秸稈以增加肥效 B.廢舊書籍、報紙分類回收,再利用 C.循環利用CO2制造合成燃料、尿素等物質 D.大力植樹造林,嚴禁亂砍濫伐森林 發布:2024/12/25 14:30:2組卷:86引用:2難度:0.9 -
3.中國承諾在2030年前實現碳達峰,2060年前實現碳中和,請回答下列問題。
(1)造成溫室效應加劇主要是因煤、和天然氣等化石燃料燃燒都會產生CO2;
(2)若CO2能合理利用,能與H2在催化劑條件下反應生成甲醇,反應的方程式為CO2+3H2X+H2O,X的化學式為催化劑;
(3)下列做法有利于實現碳中和的是。
A.積極植樹造林
B.利用風能實現清潔發電
C.大量使用一次性餐具
D.垃圾焚燒處理發布:2024/12/24 11:1:11組卷:50引用:3難度:0.6


