實驗室中要測定某無色氣體的成分,已知此氣體可能由CO2、NH3、NO2、N2、NO中的一種或幾種混合而成。將此無色氣體進行以下實驗:①先通過盛有濃硫酸的洗氣瓶,發現氣體減少一部分體積;②繼續通過裝有Na2O2固體的干燥管,發現從干燥管出來的氣體顏色呈紅棕色;③再繼續將氣體通入盛滿水倒立于水槽中的試管內,最后氣體完全被吸收,試管內仍為一滿試管液體。由此可判斷:
(1)原氣體中一定含有NH3、CO2、NONH3、CO2、NO,一定不含有N2、NO2N2、NO2。
(2)寫出②中發生反應的化學方程式2Na2O2+2CO2=2Na2CO3+O2,2NO+O2=2NO22Na2O2+2CO2=2Na2CO3+O2,2NO+O2=2NO2。
(3)由最終結果可知原氣體中CO2CO2和NONO的體積比為3:23:2。
【考點】常見氣體的檢驗.
【答案】NH3、CO2、NO;N2、NO2;2Na2O2+2CO2=2Na2CO3+O2,2NO+O2=2NO2;CO2;NO;3:2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:81引用:7難度:0.5
相似題
-
1.某無色氣體,可能含HCl、CO2、HI、SO2中的一種或幾種,將其通入氯水中,得到無色透明溶液。把溶液分成兩份,一份加入鹽酸酸化的BaCl2溶液,出現白色沉淀;另一份加入硝酸酸化的AgNO3溶液,也有白色沉淀生成。對于原無色氣體推斷一定正確的是( )
A.可能存在HCl B.一定存在SO2 C.肯定沒有CO2 D.不能肯定是否含有HI 發布:2024/12/30 7:0:1組卷:4引用:2難度:0.5 -
2.某氣體可能由CO2、SO2中的一種或兩種組成,實驗小組同學按如圖所示裝置確定該氣體的組成,將氣體從a端通入,則:

(1)B中應該裝下列試劑(填編號)
A.NaCl溶液 B.澄清石灰水 C.鹽酸 D.酸性高錳酸鉀溶液
(2)A中品紅的作用是:。
(3)D中澄清石灰水的作用是:。
(4)通過該實驗,該小組同學觀察到以下三個實驗現象:
①A中品紅褪色 ②C中品紅不褪色 ③D中澄清石灰水變渾濁
由上述現象該小組同學確認該氣體的成分為:。發布:2024/12/30 14:30:1組卷:25引用:2難度:0.7 -
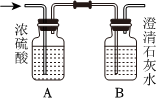 3.如圖所示,某氣體X可能由H2、CO、CH4中的一種或幾種組成.將X氣體燃燒,把燃燒后生成的氣體通過A、B兩個洗氣瓶.試回答下列問題:
3.如圖所示,某氣體X可能由H2、CO、CH4中的一種或幾種組成.將X氣體燃燒,把燃燒后生成的氣體通過A、B兩個洗氣瓶.試回答下列問題:
(1)若A洗氣瓶的質量增加,B洗氣瓶的質量不變,則氣體X是.
(2)若A洗氣瓶的質量不變,B洗氣瓶的質量增加,則氣體X是.
(3)若A、B兩個洗氣瓶的質量都增加,則氣體X可能是(可以不填滿)① ② ③ ④ ⑤ . . 發布:2024/12/30 8:0:15組卷:65引用:8難度:0.5


