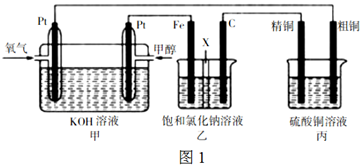
甲醇(CH3OH)是一種綠色能源。如圖1所示,某同學設計一個甲醇燃料電池并探究氯堿工業原理和粗銅的精煉原理,其中乙裝置中X為陽離子交換膜。
根據要求回答相關問題:
(1)寫出負極的電極反應式 CH3OH+8OH--6e-=CO32-+6H2OCH3OH+8OH--6e-=CO32-+6H2O。
(2)鐵電極為 陰極陰極 (填“陽極”或“陰極”),石墨電極(C)的電極反應式為 2Cl--2e-=Cl2↑2Cl--2e-=Cl2↑。
(3)若在標準狀況下,有2.24L氧氣參加反應,丙裝置中陰極析出銅的質量為 12.812.8g。
(4)若將乙裝置中兩電極位置互換,其他裝置不變,此時乙裝置中發生的總反應式 Fe+2H2O 通電 Fe(OH)2+H2↑Fe+2H2O 通電 Fe(OH)2+H2↑。
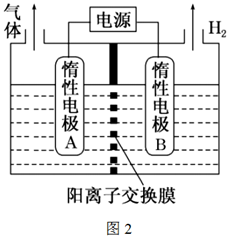
(5)2019年度的諾貝爾化學獎授予在開發鋰離子電池方面作出杰出貢獻的三位科學家。利用LiOH和鈷氧化物可制備鋰離子電池正極材料。LiOH可由電解法制備。利用如圖2所示裝置電解制備LiOH,兩電極區電解液分別為LiOH和LiCl溶液。B極區電解液為 LiOHLiOH溶液(填化學式),電解過程中Li+向 BB電極遷移(填“A”或“B”)。
通電
通電
【考點】原電池與電解池的綜合.
【答案】CH3OH+8OH--6e-=CO32-+6H2O;陰極;2Cl--2e-=Cl2↑;12.8;Fe+2H2O Fe(OH)2+H2↑;LiOH;B
通電
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/4/20 14:35:0組卷:2引用:1難度:0.5
相似題
-
1.關于如圖所示的原電池,下列說法正確的是( )
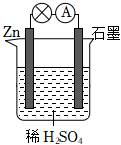
A.石墨電極上發生氧化反應 B.電子由鋅片通過導線流向石墨棒 C.該裝置將電能轉化為化學能 D.將稀硫酸換成乙醇,燈泡亮度不變 發布:2025/1/6 6:0:5組卷:83引用:5難度:0.8 -
2.某原電池結構如圖所示,下列有關該原電池的說法正確的是( )
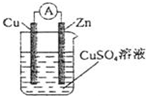
A.銅棒為負極 B.鋅棒發生還原反應 C.電子從銅棒經外電路流向鋅棒 D.鋅棒質量減輕 發布:2025/1/6 6:0:5組卷:417引用:11難度:0.9 -
3.一種新型短路膜電化學電池消除CO2裝置如圖所示。下列說法錯誤的是( )
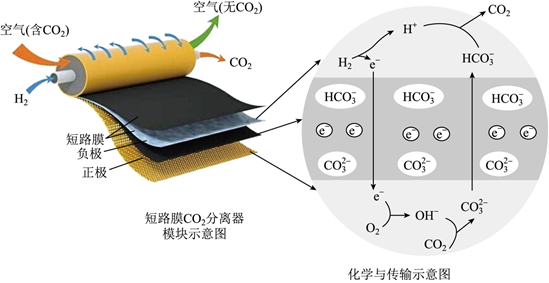
A.負極反應為:H2+2OH--2e-=2H2O B.正極反應消耗標準狀況下22.4LO2,理論上需要轉移4mol電子 C.短路膜和常見的離子交換膜不同,它既能傳遞離子,還可以傳遞電子 D.該裝置可用于空氣中CO2的捕獲,緩解溫室效應 發布:2024/12/30 19:30:2組卷:51引用:5難度:0.5


