關于堿的研究是一項重要的課題。某小組以“研究堿的部分物理和化學性質”為主題開展了以下項目式學習。
【任務一】堿的物理性質
(1)絕大多數堿為白色固體,如氫氧化鈉,但也有常溫下為液態的堿,如 氨水氨水。
【任務二】堿與部分非金屬氧化物的反應
小組同學按照圖1所示,探究水、飽和石灰水和氫氧化鈉溶液與二氧化碳反應的情況。分別將85mL液體迅速推入到圓底燒瓶中,用壓強傳感器測定,氣壓變化形成的圖像情況如圖2。
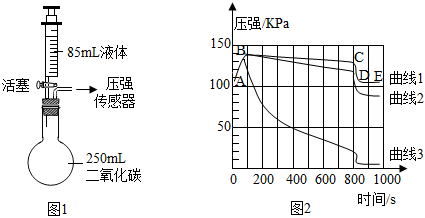
(2)圖2中,發現一開始曲線都上升(AB段),分析可能的原因是 迅速推入85mL液體,液體占據了一定的空間,氣體被壓縮,導致壓強增大迅速推入85mL液體,液體占據了一定的空間,氣體被壓縮,導致壓強增大。
(3)曲線3是 氫氧化鈉溶液氫氧化鈉溶液吸收二氧化碳變化情況,寫出該反應的化學方程式 CO2+2NaOH=Na2CO3+H2OCO2+2NaOH=Na2CO3+H2O。
(4)該實驗得到的結論是 氫氧化鈉溶液比飽和石灰水、水吸收二氧化碳能力都強(合理即可)氫氧化鈉溶液比飽和石灰水、水吸收二氧化碳能力都強(合理即可)。
【任務三】堿與酸的反應
電導率是衡量溶液導電能力大小物理量。在相同條件下,電導率與離子濃度(單位體積內的離子數)成正比,如圖3是利用數據傳感技術測定氫氧化鈉溶液與稀鹽酸反應的電導率變化過程。
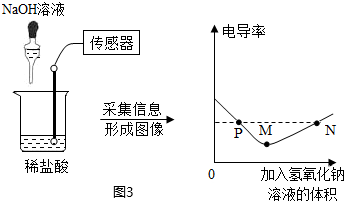
(5)M點的意義是 酸堿恰好完全反應酸堿恰好完全反應;P點和N點的電導率相同,對應溶液中的離子相同嗎?不相同不相同。為什么?P點溶液中含有的離子為Na+、H+、Cl-,N點溶液中含有的離子為Na+、OH-、Cl-(合理即可)。P點溶液中含有的離子為Na+、H+、Cl-,N點溶液中含有的離子為Na+、OH-、Cl-(合理即可)。。
【答案】氨水;迅速推入85mL液體,液體占據了一定的空間,氣體被壓縮,導致壓強增大;氫氧化鈉溶液;CO2+2NaOH=Na2CO3+H2O;氫氧化鈉溶液比飽和石灰水、水吸收二氧化碳能力都強(合理即可);酸堿恰好完全反應;不相同;P點溶液中含有的離子為Na+、H+、Cl-,N點溶液中含有的離子為Na+、OH-、Cl-(合理即可)。
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:98引用:2難度:0.6
相似題
-
1.下列物質不溶于水,但能與氫氧化鈉溶液反應的是( )
A.SiO2 B.CO2 C.MgO D.CO 發布:2024/12/25 17:30:2組卷:52引用:2難度:0.9 -
2.NaOH俗稱
,氫氧化鈉固體在空氣中易,易與空氣中反應,必須密封保存。發布:2025/1/3 8:0:1組卷:4引用:1難度:0.5 -
3.化學與生產、生活、社會息息相關,下列說法錯誤的是( )
A.熟石灰可以吸收有害氣體二氧化硫生成硫酸鈣(CaSO4) B.多用電子郵件、MSN、QQ等即時通訊工具,少用傳真打印等屬“低碳”方式 C.發射火箭采用的液氫、液氧都是無污染的純凈物 D.生活中常用加熱煮沸的方法降低水的硬度 發布:2024/12/28 8:0:1組卷:6引用:1難度:0.7


