當前位置:
試題詳情
學校化學興趣小組知道二氧化錳作過氧化氫分解的催化劑后,再想探究其它一些物質如氧化銅(CuO)是否也可作過氧化氫分解的催化劑。請你一起參與他們的探究過程,并填寫下列空白。
(1)【問題】氧化銅(CuO)能不能作過氧化氫分解的催化劑呢?
(2)【猜想】氧化銅(CuO)能作過氧化氫分解的催化劑。
(3)【實驗驗證】
| 實驗步驟 | 實驗現象 | 實驗結論 | |
| 實驗一 | 取適量過氧化氫溶液于試管中,然后將帶火星的木條伸入試管中 取適量過氧化氫溶液于試管中,然后將帶火星的木條伸入試管中
|
帶火星木條不復燃 | 常溫下過氧化氫溶液分解速率非常緩慢,放出很少量氧氣,不能使帶火星木條復燃。 |
| 實驗二 | 在裝有過氧化氫溶液的試管中加入少量(CuO),然后將帶火星的木條伸入試管中 | 有氣泡產生,帶火星木條復燃 有氣泡產生,帶火星木條復燃
|
氧化銅(CuO)能加快過氧化氫溶液的分解速率,能作為過氧化氨溶液分解的催化劑。 |
(5)【討論與反思】經過討論,有的同學認為只有上述兩個依據,不能證明氧化銅(CuO)能作過氧化氫分解的催化劑,還要補充一個探究實驗:
實驗三:
【實驗目的】探究在反應前后氧化銅的
質量是否改變
質量是否改變
。【實驗步驟】①準確稱量少量氧化銅的質量;②完成實驗二;③待反應結束,將實驗二試管里的物質進行過濾,洗滌,干燥,稱量;④對比反應前后氧化銅(CuO)的質量。
【討論】如果氧化銅(CuO)在反應前后質量不變,則說明氧化銅(CuO)可以作過氧化氫分解的催化劑。
(6)但小華認為,要證明猜想,上述三個實驗還不足夠,還需要再增加一個探究實驗:探究氧化銅(CuO)的
化學性質
化學性質
在反應前后是否改變
是否改變
。(7)通過實驗,說明了氧化銅(CuO)是過氧化氫溶液分解的催化劑。請寫出該實驗中過氧化氫溶液分解的文字表達式
過氧化氫水+氧氣
氧化銅
過氧化氫水+氧氣
。氧化銅
【考點】判斷某物質在化學反應中是否做催化劑.
【答案】取適量過氧化氫溶液于試管中,然后將帶火星的木條伸入試管中;有氣泡產生,帶火星木條復燃;質量是否改變;化學性質;是否改變;過氧化氫水+氧氣
氧化銅
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:2引用:1難度:0.5
相似題
-
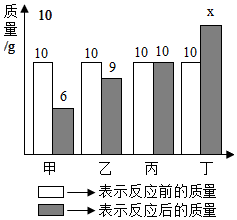 1.甲、乙、丙、丁四種物質在反應前后的質量關系如圖所示,下列有關說法錯誤的是( )
1.甲、乙、丙、丁四種物質在反應前后的質量關系如圖所示,下列有關說法錯誤的是( )A.x的值是15 B.丙可能是該反應的催化劑 C.丁是反應物 D.參加反應的甲和乙的質量比為4:1 發布:2024/8/9 8:0:9組卷:54引用:4難度:0.7 -
2.在密閉容器中加入甲、乙、丙、丁四種物質,使之充分反應,反應前后測得有關數據如表:
下列說法中,不正確的是( )物質 甲 乙 丙 丁 反應前質量/g 18 1 2 32 反應后質量/g X 26 2 12 A.反應后物質甲的質量為13g B.該反應的類型是分解反應 C.反應中乙、丁的質量比為5:4 D.丙可能是該反應的催化劑 發布:2024/8/31 3:0:11組卷:45引用:4難度:0.4 -
3.一定條件下,甲、乙、丙、丁、戊五種物質在密閉容器中發生反應,反應一段時間后,測得反應前后各種物質的質量(單位:g)如圖所示,下列說法不正確的是( )
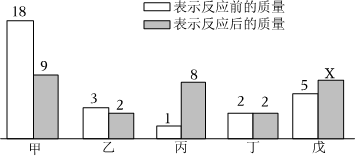 ?
?A.x的數值為8 B.丁可能是該反應的催化劑 C.反應前后乙、丙變化的質量之比為1:7 D.該反應一定是復分解反應 發布:2024/8/3 8:0:9組卷:12引用:1難度:0.5


