金屬材料的應用推動了社會發(fā)展,新型材料的研制和廢舊金屬的回收有利于節(jié)約金屬資源。
(1)三星堆出土的青銅器是迄今為止世界上絕無僅有的一類青銅器造型。青銅是銅、錫、鉛按照一定比例冶煉出來的合金,它具有 硬度大或抗腐蝕性強硬度大或抗腐蝕性強、容易鑄造等特性。
(2)被譽為“中國天眼”的PAST是目前世界上最大口徑、最靈敏的射電組遠鏡,支撐它的角鋼塔架中含有鐵、銅、錳(Mn),現(xiàn)探究三種金屬的活動性強弱。請你參與:
【猜想】猜想1:Mn>Fe>Cu;猜想2:Fe>Cu>Mn;猜想3:Fe>Mn>CuFe>Mn>Cu。
【實驗】

【分析】
Ⅰ.請寫出實驗②中的現(xiàn)象是 產生氣泡,溶液由無色變成淺綠色產生氣泡,溶液由無色變成淺綠色。
Ⅱ.實驗過程中發(fā)現(xiàn)只有實驗①無明顯現(xiàn)象,由此可得出猜想 11(填1或2或3)成立,請寫出實驗③的化學方程式:Mn+FeSO4=Fe+MnSO4Mn+FeSO4=Fe+MnSO4(反應后錳元素顯+2價)。
Ⅲ.通過實驗現(xiàn)象及分析發(fā)現(xiàn),不需要進行實驗 ④④(選填寫①②③④)就能夠得出結論。
【拓展】
已知金屬錳和鐵有相似的化學性質,能溶于稀酸,生成含有+2價金屬離子的化合物。現(xiàn)將由5.5g金屬錳、5.6g金屬鐵、6.4g金屬銅組成的混合物放入一定量的稀硫酸中,充分反應后過濾得到固體12g,同時產生氫氣的質量為 0.2g0.2g。
【考點】金屬活動性的探究.
【答案】硬度大或抗腐蝕性強;Fe>Mn>Cu;產生氣泡,溶液由無色變成淺綠色;1;Mn+FeSO4=Fe+MnSO4;④;0.2g
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:77引用:1難度:0.5
相似題
-
1.根據(jù)圖示設計的實驗來進一步認識金屬的化學性質和金屬的活動性順序。
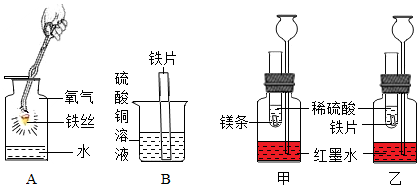
(1)寫出實驗A中反應的化學方程式:。
(2)實驗B中可觀察到鐵片的表面出現(xiàn),說明鐵的金屬活動性比銅(填“強”或“弱”)。
(3)若想探究鎂、鐵、銅三種金屬的活動性強弱,小清同學提出在實驗B的基礎上增加實驗甲和乙,便可得出結論。試管內的鎂片和鐵片表面均被打磨潔凈,且形狀、大小相同;同時加入等質量和等濃度的稀硫酸。
①乙裝置中發(fā)生反應的化學方程式為。
②觀察到試管中有氣泡產生且長頸漏斗中甲的液面上升比乙(填“快”或“慢”)時,可以證明鎂的金屬活動性比鐵的強。
③若甲、乙實驗所用的金屬均過量,則甲裝置中產生的H2質量(填“大于”“小于”或“等于”)乙裝置中產生的H2質量。
④小亮同學指出若想探究這三種金屬的活動性強弱,只需使用三種藥品即可達到實驗目的,請你幫助小亮完成其實驗方案。操作 現(xiàn)象 結論 將鎂片和銅片分別放入氯化亞鐵溶液中 放入銅片的氯化亞鐵溶液中 ,放入鎂片的氯化亞鐵溶液的顏色由金屬的活動性強弱關系為Mg>Fe>Cu 發(fā)布:2024/12/7 8:0:1組卷:77引用:1難度:0.5 -
2.2019年版第五套人民幣5角硬幣的材質已由“鋼芯鍍銅合金”改為“鋼芯鍍鎳”,其表面色澤也因此由
色變?yōu)殂y白色。化學興趣小組決定,探究制造5角硬幣的三種主要金屬(鐵、銅、鎳)活動性順序。
【查閱資料】
(1)硫酸鎳溶液顯綠色,Ni的化合價通常為+2價。
(2)鎳能與稀硫酸反應,生成硫酸鎳和氫氣。
【提出猜想】猜想①:;猜想②:Fe>Ni>Cu。
【實驗探究】
(1)甲組同學將一塊表面潔凈的鎳片放入稀硫酸中,觀察到的實驗現(xiàn)象是,有關反應的化學方程式是。
(2)乙組同學將一塊表面潔凈的鎳片浸入硫酸亞鐵溶液中,一會兒取出,發(fā)現(xiàn)鎳片表面無明顯變化,說明猜想(填“①”或“②”)成立。
(3)丙組同學用銅片、硫酸鎳溶液和進行實驗,也得出了三種金屬的活動性順序。
【拓展延伸】
(1)某電鍍公司的檢修員利用工作之便,將鎳網(wǎng)放入含有金鹽的電鍍液中偷偷“吸取”黃金,該盜竊手法利用了(填反應的基本類型)原理。該員工竊取貴重物品的行為,必將受到法律的制裁。
(2)金屬活動性實際上是金屬在水溶液中失去電子的能力大小。下列事實可以判斷M、N兩種金屬活動性順序的是(填序號)。
①M能和鹽酸反應而N不能
②M、N分別放入鹽酸中比較反應劇烈程度
③常溫下M能與氧氣反應而N不能
④M能從N的鹽溶液中置換出N發(fā)布:2024/12/25 14:0:2組卷:229引用:5難度:0.5 -
3.化學小組為探究鐵、銅、鋅、銀的金屬活動性順序,設計如下三個實驗(其中金屬均已打磨,其形狀、大小及同種稀鹽酸的用量均相同):
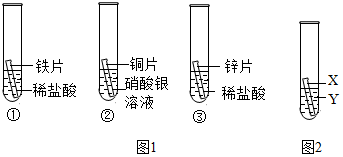
(1)實驗①的化學方程式為;一段時間后,觀察到實驗②的銅片表面有銀白色固體附著,這說明銅比銀的活動性(填“強”或“弱”)。
(2)甲同學認為通過實驗①和③可比較鋅和鐵的金屬活動性,他依據(jù)的實驗現(xiàn)象是。
(3)乙、丙兩位同學認為上述實驗方案不足以得出四種金屬的活動順序,并在上述實驗的基礎上,利用金屬
不同的化學性質分別補充了一個實驗(圖2所示),都實現(xiàn)了探究的目的。乙同學的實驗:X是金屬,Y是溶液;丙同學的實驗:X是金屬,Y是溶液。發(fā)布:2024/12/25 17:30:2組卷:45引用:4難度:0.5


