某化學興趣小組對有關SO2性質進行如圖探究活動。
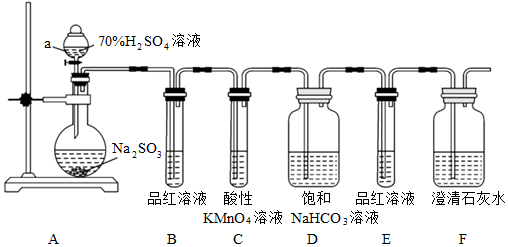
(1)實驗室通常利用Na2SO3固體與70%的H2SO4溶液反應制取SO2氣體,圖中a儀器的名稱為 分液漏斗分液漏斗,裝置A中發生反應的化學方程式為 Na2SO3+H2SO4=Na2SO4+H2O+SO2↑Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,
(2)①B中品紅溶液褪色,是因為SO2具有 漂白漂白(填“氧化”“還原”或“漂白”,下同)性,C裝置中酸性KMnO4溶液褪色,表明SO2具有 還原還原性。
②證明亞硫酸酸性比碳酸酸性強的實驗現象是 E中品紅溶液不變色,F中澄清石灰水變渾濁E中品紅溶液不變色,F中澄清石灰水變渾濁;
③若將SO2氣體直接通入澄清石灰水中,溶液變渾濁,則該反應的離子方程式為 SO2+Ca2++2OH一=CaSO3↓+H2OSO2+Ca2++2OH一=CaSO3↓+H2O。
【考點】二氧化硫的性質.
【答案】分液漏斗;Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;漂白;還原;E中品紅溶液不變色,F中澄清石灰水變渾濁;SO2+Ca2++2OH一=CaSO3↓+H2O
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:133引用:2難度:0.5
相似題
-
1.下列敘述中,正確的是( )
A.SO2在空氣中易被氧化為SO3 B.SO2大量應用于食品消毒和漂白 C.SO2與SO3都能與水劇烈反應 D.SO2可用于漂白紙漿,SO3不能 發布:2024/12/30 15:0:1組卷:8引用:2難度:0.7 -
2.因為SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性
.(判斷對錯)發布:2024/12/30 19:30:2組卷:39引用:2難度:0.9 -
3.近年來,總有一些不法商販為了牟取自身利益。用硫磺(燃燒硫磺)對銀耳進行熏制,使銀耳增白。這些不法商販所制取的銀耳是利用了( )
A.SO2的氧化性 B.S的漂白性 C.SO2的漂白性 D.SO2的還原性 發布:2025/1/6 7:30:5組卷:30引用:3難度:0.5


