(1)依據反應:Cu2++Zn(s)=Zn2+(aq)+Cu(s)設計的原電池如圖甲所示。
①電極X的材料是 ZnZn;Y溶液可以是 硫酸銅溶液硫酸銅溶液。
②Cu電極上發生的電極反應式是 Cu2++2e-=CuCu2++2e-=Cu。
③電池放電時,電子從電極 ZnZn經電流計流向電極 CuCu。(填電極材料)
④電池放電過程中,盛有飽和KCl瓊脂溶膠的鹽橋中,向ZnSO4溶液一端擴散的離子是 Cl-Cl-(填離子符號)。
(2)鋼鐵發生電化學腐蝕可分為析氫腐蝕和吸氧腐蝕,可以采用電化學手段進行防腐。
①寫出鋼鐵在酸性較強的環境中發生電化學腐蝕的正極反應式:2H++2e-=H2↑2H++2e-=H2↑。
②為了減緩水庫鐵閘門被腐蝕的速率,可以采用圖乙所示的方案,其中連接在鐵閘門上的固體材料R可以采用(填寫字母序號) CC。
A.銅
B.鈉
C.鋅
D.石墨
③圖丙所示方案也可以減緩鐵閘門的腐蝕速率,則石墨應連接直流電源的 正正極。

(3)電解原理在工業上有著廣泛的用途,如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連。
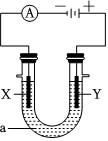
①若X、Y都是惰性電極,a是飽和NaCl溶液,則:X極上的電極反應式為 2H2O+2e-=H2↑+2OH-2H2O+2e-=H2↑+2OH-;Y電極上的電極反應式為 2Cl--2e-=Cl2↑2Cl--2e-=Cl2↑。
②如要用電解方法精煉粗銅,電解液a選用CuSO4溶液,則:X電極的材料是 純銅純銅(填粗銅或純銅)。Y電極上主要的電極反應式 Cu-2e-=Cu2+Cu-2e-=Cu2+。
【答案】Zn;硫酸銅溶液;Cu2++2e-=Cu;Zn;Cu;Cl-;2H++2e-=H2↑;C;正;2H2O+2e-=H2↑+2OH-;2Cl--2e-=Cl2↑;純銅;Cu-2e-=Cu2+
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:16引用:1難度:0.5
相似題
-
1.關于如圖所示的原電池,下列說法正確的是( )
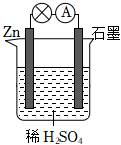
A.石墨電極上發生氧化反應 B.電子由鋅片通過導線流向石墨棒 C.該裝置將電能轉化為化學能 D.將稀硫酸換成乙醇,燈泡亮度不變 發布:2025/1/6 6:0:5組卷:83引用:5難度:0.8 -
2.某原電池結構如圖所示,下列有關該原電池的說法正確的是( )
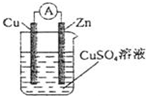
A.銅棒為負極 B.鋅棒發生還原反應 C.電子從銅棒經外電路流向鋅棒 D.鋅棒質量減輕 發布:2025/1/6 6:0:5組卷:417引用:11難度:0.9 -
3.一種新型短路膜電化學電池消除CO2裝置如圖所示。下列說法錯誤的是( )
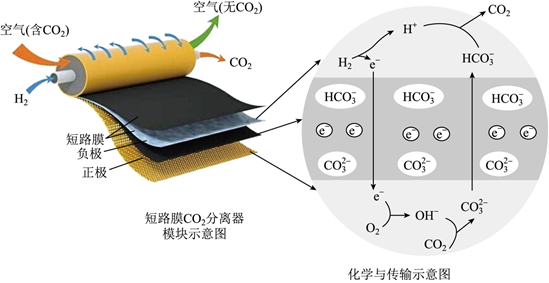
A.負極反應為:H2+2OH--2e-=2H2O B.正極反應消耗標準狀況下22.4LO2,理論上需要轉移4mol電子 C.短路膜和常見的離子交換膜不同,它既能傳遞離子,還可以傳遞電子 D.該裝置可用于空氣中CO2的捕獲,緩解溫室效應 發布:2024/12/30 19:30:2組卷:51引用:5難度:0.5


