在實驗室制取CO2,同學們圍繞驗滿CO2展開了如下探究活動。
【提出問題】利用如圖裝置A收集CO2時,如何判斷CO2收集滿了?
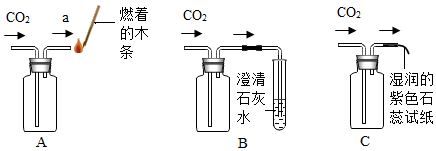
【設計并實驗】根據CO2具有不燃燒、也不支持燃燒不燃燒、也不支持燃燒的化學性質,可將燃著的木條放在裝置A的a端導管口處,當觀察到木條立即熄滅即可判斷CO2已經收集滿。但在多次驗滿CO2實驗過程中,發現燃著的木條持續燃燒了很長時間才熄滅,或者根本不熄滅。
【表達與交流】同學們一致認為:用燃著的木條來驗滿裝置A中是否收集滿CO2是不可靠的。
【設計并實驗】經過討論,同學們重新設計了兩種方法并進行實驗驗證:
方法一:如圖裝置B,在實驗過程中很快觀察到澄清石灰水變渾濁了,由此判斷已收集滿CO2。試管中發生反應的化學方程式為Ca(OH)2+CO2=CaCO3↓+H2OCa(OH)2+CO2=CaCO3↓+H2O。
方法二:如圖裝置C,在實驗過程中很快觀察到濕潤的紫色石蕊試紙變紅色濕潤的紫色石蕊試紙變紅色現象,由此判斷已收集滿CO2。
【實驗反思】通過以上探究活動,我們得到的啟示有下列中的BCBC。
A.根據物質的性質預測出的實驗現象與實際實驗產生的實驗現象一定是一致的
B.通過動手實驗,可以幫助我們分析和解決化學問題
C.合作與交流在科學探究中具有重要作用
【答案】不燃燒、也不支持燃燒;Ca(OH)2+CO2=CaCO3↓+H2O;濕潤的紫色石蕊試紙變紅色;BC
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:130引用:2難度:0.5
相似題
-
1.實驗室制取氣體所需的裝置如圖所示,請回答以下問題。
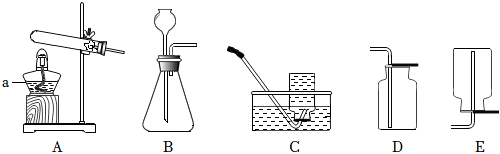
(1)a儀器名稱。收集氧氣可以選用C,原因是。用高錳酸鉀制氧氣,反應的化學方程式為。
(2)實驗室用石灰石和稀鹽酸制取CO2,發生裝置應選用,收集用,CO2的驗滿方法為。發布:2024/12/8 10:30:2組卷:50引用:4難度:0.5 -
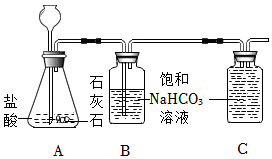 2.實驗室可用如圖裝置制取二氧化碳;已知常溫下CO2灘溶于飽和NaHCO3溶液。
2.實驗室可用如圖裝置制取二氧化碳;已知常溫下CO2灘溶于飽和NaHCO3溶液。
(1)寫出A裝置中發生反應的化學方程式。
(2)B中飽和碳酸氫鈉溶液的作用是什么?
(3)利用排飽和NaHCO3溶液法可以收集較純凈的二氧化碳氣體,請將C裝置中的導管補畫完整。發布:2024/12/25 15:0:2組卷:7引用:2難度:0.6 -
3.用圖-1所示裝置制取干燥的CO2,并對CO2的部分性質進行探究。
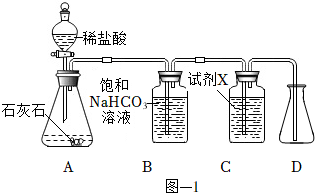
(1)裝置A中發生反應的化學方程式為。
(2)①裝置B中飽和NaHCO3溶液的作用是。
②裝置C中試劑X應該選用(填字母)。
a.稀H2SO4
b.濃H2SO4
c.KOH溶液
(3)收集CO2并驗滿。將集滿CO2的錐形瓶與盛有足量NaOH溶液的注射器和傳感器密封連接,緩慢的將NaOH溶液注入到錐形瓶中,采集信息形成圖像。見圖-2。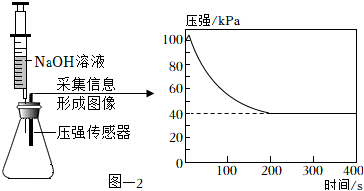
①檢驗裝置D中CO2已經集滿的方法是。
②隨著反應的進行,錐形瓶中壓強降低的原因是。
③反應結束后錐形瓶中的壓強保持在40kPa說明。
(4)取2mL飽和澄清石灰水于試管中,用4mL蒸餾水稀釋,向其中緩慢通入足量CO2。測定反應體系的電導率變化如圖-3所示。(忽略反應前后溶液體積的變化)
【查閱資料】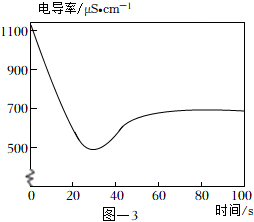
材料一:溶液的導電能力越強,溶液的電導率越大。
材料二:單位體積溶液中某離子的個數越多,則該離子的濃度越大,溶液的導電能力越強。相同濃度的不同離子導電能力不同。
材料三:Ca( OH)2溶于水能完全解離出Ca2+和OH-。
CaCO3遇到溶有CO2的水時,能反應生成易溶于水的Ca( HCO3)2,Ca( HCO3)2在水中能完全解離出Ca2+和。HCO-3
①石灰水中通入CO2氣體,溶液的電導率先逐漸降低的主要原因是。
②反應最終電導率的穩定值低于初始值的可能原因是、。發布:2024/12/25 13:0:1組卷:841引用:3難度:0.6


