(NH4)2S2O8電化學循環氧化法可用于廢水中苯酚的降解,示意圖如圖。
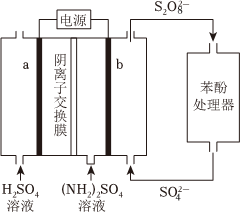
(1)(NH4)2S2O8的電解法制備。
已知:電解效率η的定義為η(B)=n(生成B所用的電子)n(通過電極的電子)×100%。
①電極b是 陽陽極。
②生成S2O2-8 的電極反應式是 2SO42--2e-=S2O82-2SO42--2e-=S2O82-。
③向陽極室和陰極室各加入100mL溶液。制備S2O2-8的同時,還在電極b表面收集到2.5×10-4mol氣體,氣體是 O2O2。經測定η(S2O2-8)為80%,不考慮其他副反應,則制備的(NH4)2S2O8的物質的量濃度為 0.020.02mol/L。
(2)苯酚的降解
已知:SO-4?具有強氧化性,Fe2+性度較高時會導致SO-4?猝滅。S2O2-8可將苯酚氧化為CO2,但反應速率較慢。加入Fe2+可加快反應,過程為:
i.S2O2-8+Fe2+═SO2-4+SO-4?+Fe3+
ii.SO-4?將苯酚氧化
①SO-4?氧化苯酚的離子方程式是  ++28SO-4?+11H2O→6CO2+28SO42-+28H+
++28SO-4?+11H2O→6CO2+28SO42-+28H+ ++28SO-4?+11H2O→6CO2+28SO42-+28H+。
++28SO-4?+11H2O→6CO2+28SO42-+28H+。
②將電解得到的含S2O2-8溶液稀釋后加入苯酚處理器,調節溶液總體積為1L,pH=1,測得在相同時間內,不同條件下苯酚的降解率如圖。
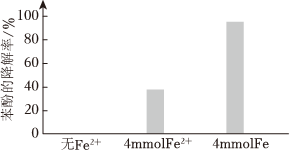
用等物質的量的鐵粉代替FeSO4,可明顯提高苯酚的降解率,主要原因是 Fe緩慢釋放Fe2+,使(Fe2+)較低,減弱了Fe2+對SO-4?的猝滅作用;且Fe可以和產生的Fe3+反應,繼續補充Fe2+Fe緩慢釋放Fe2+,使(Fe2+)較低,減弱了Fe2+對SO-4?的猝滅作用;且Fe可以和產生的Fe3+反應,繼續補充Fe2+。
(3)苯酚殘留量的測定
已知:電解中轉移1mol電子所消耗的電量為F庫侖。
取處理后的水樣100mL,酸化后加入KBr溶液,通電。電解產生的Br2全部與苯酚反應,當苯酚完全反應時,消耗的電量為a庫侖,則樣品中苯酚的含量為 940a6F940a6Fg/L。(苯酚的摩爾質量:94g/mol)
n
(
生成
B
所用的電子
)
n
(
通過電極的電子
)
O
2
-
8
2
SO
4
2
-
-
2
e
-
=
S
2
O
8
2
-
2
SO
4
2
-
-
2
e
-
=
S
2
O
8
2
-
O
2
-
8
O
2
-
8
SO
-
4
SO
-
4
O
2
-
8
O
2
-
8
SO
2
-
4
SO
-
4
SO
-
4
SO
-
4
 ++28
++28SO
-
4
6
CO
2
+
28
S
O
4
2
-
+
2
8
H
+
 ++28
++28SO
-
4
6
CO
2
+
28
S
O
4
2
-
+
2
8
H
+
O
2
-
8
SO
-
4
SO
-
4
940
a
6
F
940
a
6
F
【答案】陽;;O2;0.02; ++28?+11H2O→;Fe緩慢釋放Fe2+,使(Fe2+)較低,減弱了Fe2+對?的猝滅作用;且Fe可以和產生的Fe3+反應,繼續補充Fe2+;
++28?+11H2O→;Fe緩慢釋放Fe2+,使(Fe2+)較低,減弱了Fe2+對?的猝滅作用;且Fe可以和產生的Fe3+反應,繼續補充Fe2+;
2
SO
4
2
-
-
2
e
-
=
S
2
O
8
2
-
 ++28
++28SO
-
4
6
CO
2
+
28
S
O
4
2
-
+
2
8
H
+
SO
-
4
940
a
6
F
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/12/30 11:30:1組卷:161引用:2難度:0.4
相似題
-
1.利用微生物處理有機廢水,可在獲得電能的同時實現海水淡化。現以NaCl溶液模擬海水,采用惰性電極,用圖甲所示裝置處理含CH3COO-的有機廢水,并用該裝置在鐵上鍍銅(如圖乙),下列說法不正確的是( )
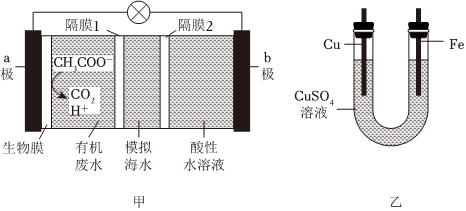
A.a極生物膜上發生的電極反應為:CH3COO--8e-+2H2O═2CO2+7H+ B.隔膜1為陰離子交換膜,隔膜2為陽離子交換膜 C.電極b應與銅棒相連,CuSO4溶液濃度基本保持不變 D.當生成1molCO2時,模擬海水理論上除鹽117g 發布:2024/12/20 16:0:2組卷:174引用:3難度:0.5 -
2.鈰(Ce)是鑭系金屬元素。空氣污染物NO通常用含Ce4+的溶液吸收,生成HNO2、
,再利用電解法將上述吸收液中的HNO2轉化為無毒物質,同時生成Ce4+,其原理如圖所示。下列說法正確的是( )NO-3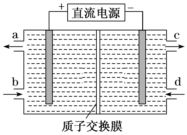
A.H+由右室進入左室 B.Ce4+從電解槽的c口流出,且可循環使用 C.陰極的電極反應式:2HNO2+6H++6e-═N2↑+4H2O D.若用甲烷燃料電池作為電源,當消耗標準狀況下33.6L甲烷時,理論上可轉化2mol HNO2 發布:2025/1/6 7:30:5組卷:129引用:7難度:0.7 -
3.如圖所示,某同學設計一個甲醚(CH3OCH3)燃料電池并探究氯堿工業原理和粗銅的精煉原理,其中乙裝置中X為陽離子交換膜。
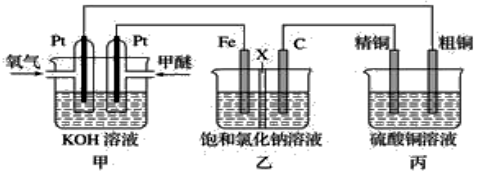
(1)通入氧氣的電極為極,寫出負極電極反應式。
(2)鐵電極為極,石墨電極(C)的電極反應式為。
(3)反應一段時間后,乙裝置中生成NaOH主要在(填“鐵極”或“石墨極”)區。
(4)如果粗銅中含有鋅、銀等雜質,丙裝置中陽極上電極反應式為,反應一段時間,硫酸銅溶液濃度將(填“增大”、“減小”或“不變”)發布:2025/1/3 8:0:1組卷:6引用:1難度:0.6
相關試卷


