Ⅰ.鐵元素在地殼中含量居于第四位。鐵是目前產量最大,使用最廣泛的金屬。我國目前發現最早的人工冶鐵制品是河南三門峽出土的西周晚期的玉柄鐵劍。
(1)在鋼鐵廠的生產中,熾熱的鐵水或鋼水注入模具之前必須進行充分的干燥處理,不得留有水,請用化學方程式解釋 3Fe+4H2O(g) 高溫 Fe3O4+4H23Fe+4H2O(g) 高溫 Fe3O4+4H2。
(2)鐵是人體必需微量元素中含量最多的一種。當人體貧血時,可以服用含FeSO4的補血劑,搭配維C效果更好,維C在這個過程中的作用是做 還原還原劑。
(3)電子工業中常用FeCl3溶液作為“腐蝕液”腐蝕覆銅板。為了檢驗反應后所得混合溶液中還有Fe3+,可選擇下列試劑中的 AA(填編號,下同)進行檢驗,現象是 溶液變為紅色溶液變為紅色。
A.KSCN溶液
B.酸性KMnO4溶液
C.新制氯水
(4)高鐵酸鈉(Na2FeO4)是一種新型綠色消毒劑,其一種制備原理如下:33ClO-+22Fe3++10OH-10OH-=22FeO2-4+33Cl-+55H2O。請將方程式補充完整并配平該方程式。
Ⅱ.氯是一種重要的成鹽元素,在自然界中主要以NaCl的形式大量存在于海水中。氯的單質氯氣是一種重要的化工原料。實驗室利用如圖所示裝置制取并收集氯氣: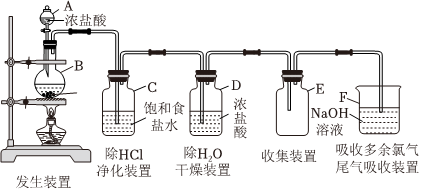
(5)裝置A的名稱是 分液漏斗分液漏斗。
(6)氯氣除了可以用向上排空氣法收集,還可以用排 飽和食鹽水飽和食鹽水溶液的方法收集。
Ⅲ.元素周期表是學習化學的重要工具,它揭示了元素間的內在聯系。
(7)鹵素是元素周期表中第ⅦA族元素,按F、Cl、Br、I的順序非金屬性逐漸減弱,下列關于鹵素的說法錯誤的是 BDBD。
A.單質顏色隨核電荷數的增加而加深
B.氫化物的穩定性隨核電荷數的增加而增大
C.原子半徑隨核電荷數的增加而增大
D.單質的氧化性隨核電荷數的增大而增強
高溫
高溫
F
e
O
2
-
4
【答案】3Fe+4H2O(g) Fe3O4+4H2;還原;A;溶液變為紅色;3;2;10OH-;2;3;5;分液漏斗;飽和食鹽水;BD
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:33引用:1難度:0.7
相似題
-
1.為了驗證干燥的氯氣無漂白性,濕潤的氯氣具有漂白性,某同學設計實驗如圖.其中B、C、D、E、F分別盛有飽和食鹽水、濃硫酸.干燥紅色布條、濃硫酸、濕潤紅色布條.
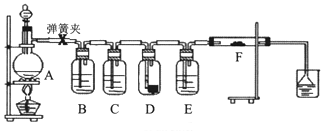
請回答:
(1)E中濃硫酸的作用.
(2)將F中的濕潤布條換成卷曲的細銅絲,并用酒精燈加熱,可看到的現象是.
(3)若用裝置A制取2.24L(標況)氯氣,消耗10mol/L濃鹽酸的體積明顯大于40mL,造成該結果的可能原因有.
A.濃鹽酸的揮發 B.隨反應進行鹽酸濃度下降
C.加熱時火力不夠猛 D.MnO2固體過量.發布:2025/1/15 8:0:2組卷:17引用:1難度:0.3 -
2.如圖是某同學設計的氯氣制備及性質驗證實驗裝置。相關說法正確的是( )

A.脫脂棉中的無水氯化鈣可以用堿石灰代替 B.該實驗裝置可證明干燥的氯氣沒有漂白作用 C.濕潤的紫色石蕊試紙變紅色,說明反應生成了酸性物質 D.濕潤的淀粉碘化鉀試紙變藍色,然后又逐漸褪去,說明氯氣具有漂白性 發布:2025/1/15 8:0:2組卷:20引用:2難度:0.8 -
3.實驗室中模擬用甲烷與氯氣反應得到的副產品來制取鹽酸,原理如圖,下列說法不正確的是( )
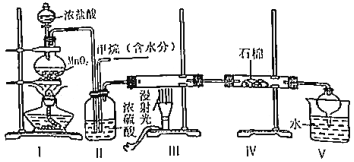
A.依據裝管Ⅰ中的現象控制氣流的速度 B.分離裝置V中鹽酸的最佳操作方法是分液 C.裝置Ⅳ的石棉中可加入一些氫氧化鈉粉末 D.實驗過程中可觀察到裝置Ⅲ中硬質玻璃管內壁有附著的油珠 發布:2024/12/30 17:0:5組卷:61引用:1難度:0.7


