當前位置:
試題詳情
 通過晾曬海水或煮鹽井水、鹽湖水等,可以蒸發除去其水分,得到含有較多雜質的氯化鈉晶體——粗鹽。
通過晾曬海水或煮鹽井水、鹽湖水等,可以蒸發除去其水分,得到含有較多雜質的氯化鈉晶體——粗鹽。
小剛在實驗室做粗鹽提純實驗的操作如下:
步驟1:用托盤天平稱取10g粗鹽,用藥匙將粗鹽逐漸加入盛有20mL水的燒杯里,邊加邊用玻璃棒攪拌,直到粗鹽不再溶解為止。稱量剩余粗鹽的質量為2.8g。
(1)玻璃棒在上述操作中的作用是 加快溶解速率加快溶解速率。
(2)如果第一次稱量前,托盤天平忘記調節平衡,指針偏向右邊(第二次稱量正常),實際加到燒杯里的粗鹽 BB。
A.等于7.2g
B.大于7.2g
C.小于7.2g
D.無法判斷
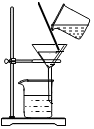
步驟2:制作過濾裝置,如圖所示,過濾步驟1中燒杯里的混合物。
(3)制作過濾裝置所需儀器有 鐵架臺(帶鐵圈)、燒杯、漏斗、玻璃棒鐵架臺(帶鐵圈)、燒杯、漏斗、玻璃棒。
(4)進行過濾的目的是 除去難溶于水的物質除去難溶于水的物質。
(5)如果濾液仍渾濁,其可能的原因是 濾紙破損、液面高于濾紙邊緣、承接濾液的燒杯不潔凈等濾紙破損、液面高于濾紙邊緣、承接濾液的燒杯不潔凈等。
步驟3:把所得澄清濾液倒入蒸發皿,把蒸發皿放在鐵架臺的鐵圈上,用酒精燈加熱,同時用玻璃棒不斷攪拌濾液,待蒸發皿中出現較多量固體時停止加熱,烘干、稱量得3.6g固體。
(6)玻璃棒攪拌濾液的目的是 使液體均勻受熱,防止液體飛濺使液體均勻受熱,防止液體飛濺。
(7)小剛的粗鹽提純產率是 50%50%。
(8)請分析該產率是否就是粗鹽中所含NaCl的質量分數?否,是因為氯化鈉中仍然含有溶于水的物質否,是因為氯化鈉中仍然含有溶于水的物質。
【答案】加快溶解速率;B;鐵架臺(帶鐵圈)、燒杯、漏斗、玻璃棒;除去難溶于水的物質;濾紙破損、液面高于濾紙邊緣、承接濾液的燒杯不潔凈等;使液體均勻受熱,防止液體飛濺;50%;否,是因為氯化鈉中仍然含有溶于水的物質
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/5/23 20:38:36組卷:10引用:2難度:0.5
相似題
-
 1.去除難溶性雜質后的食鹽樣品中還含有可溶性雜質:CaCl2、MgCl2和Na2SO4.為除去可溶性雜質,將食鹽樣品溶于水,依次加入稍過量的三種溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反應后過濾,得濾渣X,向濾液中加入過量的稀鹽酸,攪拌、煮沸,得氯化鈉溶液。下列說法正確的是( )
1.去除難溶性雜質后的食鹽樣品中還含有可溶性雜質:CaCl2、MgCl2和Na2SO4.為除去可溶性雜質,將食鹽樣品溶于水,依次加入稍過量的三種溶液:BaCl2溶液、NaOH溶液、Na2CO3溶液。充分反應后過濾,得濾渣X,向濾液中加入過量的稀鹽酸,攪拌、煮沸,得氯化鈉溶液。下列說法正確的是( )A.濾渣X中有三種成分 B.“向濾液中加入過量的稀鹽酸”目的只是為了除去過量的NaOH C.除雜過程中有Na2CO3參加的化學反應為復分解反應 D.將氯化鈉溶液用題圖裝置加熱蒸發,至水分完全蒸干時停止加熱 發布:2024/12/25 15:30:1組卷:741引用:8難度:0.5 -
2.在“粗鹽的初步提純”實驗中,下列操作正確的是( )
A. 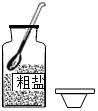
取用B. 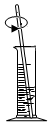
溶解C. 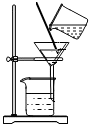
過濾D. 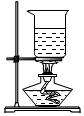
蒸發發布:2024/12/25 16:0:1組卷:136引用:3難度:0.7 -
3.多角度認識溶液,有助于我們更好地了解其在生產生活中的重要作用.
(1)物質在水中的分散
①食鹽是重要的調味品,其主要成分氯化鈉是由構成的(選填“分子”、“原子”或“離子”),將適量食鹽加入水中,充分攪拌后能形成溶液.
②食用油加入水中,充分攪拌能形成乳濁液.洗潔精洗滌油膩的碗筷是利用原理.
③面粉加入水中,充分攪拌后能形成懸濁液.除去懸濁液中難溶性的面粉可用的操作方法是.
(2)溶液的性質
①關于溶液的說法正確的有(填標號).
A.鹽酸是純凈物 B.溶液是均一、穩定的
C.溶液的酸堿度可用石蕊溶液測定 D.飽和溶液不一定是濃溶液
②有些固體物質溶解形成溶液后會呈現不同的顏色,如品紅溶液是紅色的,放入活性炭可使紅色褪去,這利用活性炭的作用.
③a,b兩種物質的溶解度曲線如圖1所示.下列說法正確的是
A.a物質的溶解度一定大于b物質的溶解度
B.將a溶液從t2℃時降溫到t1℃時,一定有晶體析出
C.t1℃時,a、b兩種物質飽和溶液的溶質質量分數相等
D.將t2℃時b的飽和溶液變為不飽和溶液,可采取降溫的方法
(3)溶液的變化
將一定質量的飽和氯化鈉溶液通電一段時間后,下列敘述正確的是
通電
(反應原理為:2NaCl+2H2O═2NaOH+H2↑+Cl2↑)
A.溶液的pH逐漸減小 B.溶液中鈉元素的質量增大
C.溶液中氧元素的質量分數不變 D.氯化鈉溶液的溶質質量分數減小
(4)如圖2是“粗鹽中難溶性雜質的去除”的實驗操作示意圖:
①儀器a的名稱.
②操作A中托盤兩邊各放一張大小相同的紙片,其作用是.
③操作B中還需要用到的儀器是.
④操作 C過濾時倒入液體的液面要低于濾紙邊緣主要是為了防止(填字母).
A.過濾速度慢 B.濾紙破損 C.雜質未經過濾就進入濾液
⑤圖中部分操作有錯誤,其中有的錯誤會導致精鹽產率明顯偏低,其原因是.發布:2025/1/1 8:0:2組卷:55引用:1難度:0.5


