 某化學學習小組的同學 依據(jù)氧化還原反應:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,可采用滴定的方法測定FeSO4的質(zhì)量分數(shù),實驗步驟如下:
某化學學習小組的同學 依據(jù)氧化還原反應:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,可采用滴定的方法測定FeSO4的質(zhì)量分數(shù),實驗步驟如下:
①稱量綠礬樣品30.4g,配成100mL待測溶液
②取10.0mL待測液置于錐形瓶中,并加入一定量的硫酸
③將0.1mol?L-1的KMnO4溶液裝入滴定管中,調(diào)節(jié)液面至8.00mL處
④滴定待測液至滴定終點時,滴定管的液面讀數(shù)18.00mL(其中的雜質(zhì)不跟高錳酸鉀和稀硫酸反應).請回答下列問題:
(1)滴定時用甲甲(填右圖的“甲”或“乙”)滴定管盛裝KMnO4標準溶液;
(2)滴定前是否要滴加指示劑?否否(填“是”或“否”),請說明理由高錳酸鉀本身呈紫色,被還原后溶液會變成無色高錳酸鉀本身呈紫色,被還原后溶液會變成無色;
(3)本實驗達到終點的標志是滴入最后一滴KMnO4溶液恰好由黃綠色變淺紫紅色,且半分鐘內(nèi)不褪色滴入最后一滴KMnO4溶液恰好由黃綠色變淺紫紅色,且半分鐘內(nèi)不褪色;
(4)樣品中FeSO4的質(zhì)量分數(shù)為25%25%;
(5)誤差分析(選填“偏高”“偏低”或“無影響”)
①開始實驗時酸式滴定管尖嘴處有氣泡,在滴定過程中氣泡消失偏高偏高
②若滴定前仰視滴定管刻度讀數(shù)時,則會使滴定結(jié)果偏低偏低.
【考點】中和滴定.
【答案】甲;否;高錳酸鉀本身呈紫色,被還原后溶液會變成無色;滴入最后一滴KMnO4溶液恰好由黃綠色變淺紫紅色,且半分鐘內(nèi)不褪色;25%;偏高;偏低
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:14引用:1難度:0.5
相似題
-
1.下列實驗方法或操作正確的是( )
A.酸堿中和滴定時,右手旋轉(zhuǎn)滴定管的活塞,左手搖動錐形瓶,眼睛注視滴定管中的液面 B.用200mL燒杯配制物質(zhì)的量濃度約為0.1000mol/L氫氧化鈉溶液200mL C.不用另加任何試劑就能鑒別NaAlO2、Na2SiO3、HCl、NaCl四種無色溶液 D.用托盤天平稱取1.6g硫酸銅晶體配制100mL 0.1mol/L的硫酸銅溶液 發(fā)布:2024/12/12 8:0:1組卷:9引用:1難度:0.7 -
2.下面關于中和滴定的實驗操作敘述不正確的有( )
①將錐形瓶用蒸餾水和待測定的鹽酸溶液進行洗滌
②取20mL待測定的鹽酸溶液,注入錐形瓶中
③向錐形瓶中加入幾滴酚酞試液為指示劑
④堿式滴定管用蒸餾水洗滌后,直接注入已知濃度的NaOH溶液
⑤進行中和滴定時,一旦錐形瓶內(nèi)溶液由無色變成粉紅色,即可停止滴定
⑥記錄數(shù)據(jù),進行必要的數(shù)據(jù)處理和得出結(jié)論A.①④⑥ B.①②④ C.①②④⑤ D.②③⑤ 發(fā)布:2024/12/10 0:30:1組卷:92引用:2難度:0.7 -
3.食醋是日常飲食中的一種調(diào)味劑,國家標準規(guī)定釀造食醋中醋酸含量不得低于0.035g/mL,實驗室用標準NaOH溶液測定食醋中醋酸的濃度,以檢測食醋是否符合國家標準,某品牌白醋的醋酸濃度測定過程如圖所示,請回答:
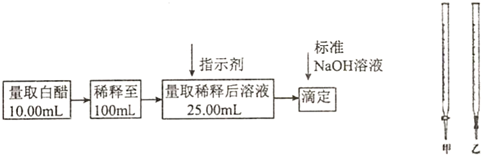
(1)選用上述(填“甲”或“乙”)滴定管量取10.00mL白醋后,將白醋稀釋至100mL時,需要使用的玻璃儀器有燒杯、玻璃棒和.
(2)某同學用酸堿中和滴定法測定該品牌白醋的醋酸濃度,當醋酸與氫氧化鈉恰好完全反應時,測得溶液中=c(CH3COOH)c(CH3COO-),則此時溶液中的pH=11.8×103.(已知:室溫下醋酸的Ka=1.8×10-5)
(3)根據(jù)該同學的計算結(jié)果,應該選作指示劑.(填“酚酞”、“甲基橙”或“石蕊”)
(4)該滴定達到終點時的現(xiàn)象是.
(5)某次實驗滴定開始和結(jié)束時,堿式滴定管中的液面如下圖所示,則所用NaOH溶液的體積為mL.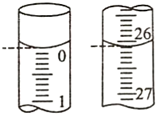
(6)用標準的0.06000mol?L-1NaOH溶液滴定上述稀釋后的醋酸溶液,滴定結(jié)果如下表所示:
則該品牌白醋中醋酸含量為滴定次數(shù) 待測溶液的體積/mL 標準溶液的體積 滴定前刻度/mL 滴定后刻度/mL 1 25.00mL 0.02 25.01 2 25.00mL 0.70 25.71 3 25.00mL 0.50 24.2 mg/mL.
(7)下列操作中,可能使所測白醋中醋酸的濃度數(shù)值偏高的是.(填編號)
A.取待測液的滴管,取液前滴定管尖嘴處無氣泡,取液后尖嘴處出現(xiàn)氣泡
B.滴定前盛放白醋稀溶液的錐形瓶用蒸餾水洗凈后沒有干燥
C.堿式滴定管未用標準NaOH溶液潤洗就直接注入標準NaOH溶液
D.讀取NaOH溶液體積時,開始時俯視讀數(shù),滴定結(jié)束時仰視讀數(shù)
(8)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度處,現(xiàn)把管內(nèi)液體全部放出,用量筒接收,得到溶液的體積是.
A.等于10mL
B.等于40mL
C.大于40mL
D.不能確定發(fā)布:2024/12/30 3:0:4組卷:54引用:2難度:0.6


