當前位置:
試題詳情
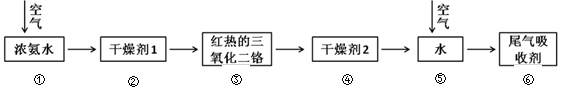
硝酸是重要的化工產品,硝酸的工業制法包括氨氣的催化氧化等步驟。模仿硝酸的工業制備過程,在實驗室通過簡單的裝置可制備硝酸。以下為實驗室制備硝酸的流程圖(已知三氧化二鉻用作催化劑,干燥劑2為濃硫酸):
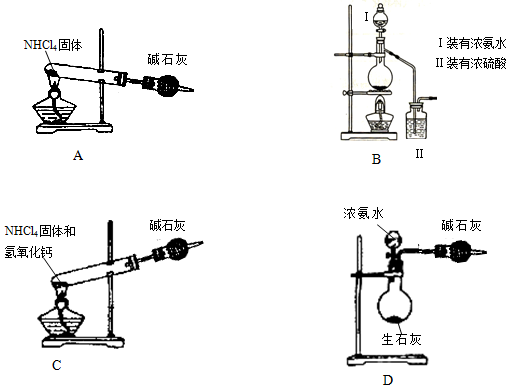
(1)下面哪套裝置可以代替流程圖中①和②的作用DD
(2)①中濃氨水可揮發出氨氣,實驗室檢驗氨氣的方法是用玻璃棒蘸取一張濕潤的紅色石蕊試紙至于濃氨水上方,試紙由紅色變成藍色,說明有氨氣揮發用玻璃棒蘸取一張濕潤的紅色石蕊試紙至于濃氨水上方,試紙由紅色變成藍色,說明有氨氣揮發。(要求寫出操作、現象與結論)
(3)③中發生的化學反應是氨氣的催化氧化,寫出反應方程式4NH3+5O2催化劑△4NO+6H2O4NH3+5O2催化劑△4NO+6H2O。
(4)反應一段時間后,觀察到③中物質呈紅熱狀態;停止加熱后仍能保持紅熱,該反應是放熱放熱 反應(填“吸熱”或“放熱”)。
(5)通過紅熱的三氧化二鉻后反應后的氣體仍然是混合氣體,其成分除了空氣外,還有NH3、NO、NO2NH3、NO、NO2。
(6)盛有Na2CO3溶液的燒杯為尾氣處理裝置,該裝置中反應的化學反應方程式是
22NO2+11Na2CO3═11NaNO2+11CO2+□1NaNO31NaNO3(請在橫線上補充另外一種產物并在橫線內配平出相關系數,系數為1也要標出)
催化劑
△
催化劑
△
【考點】工業制取硝酸.
【答案】D;用玻璃棒蘸取一張濕潤的紅色石蕊試紙至于濃氨水上方,試紙由紅色變成藍色,說明有氨氣揮發;4NH3+5O24NO+6H2O;放熱;NH3、NO、NO2;2;1;1;1;1NaNO3
催化劑
△
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/11/2 8:0:1組卷:72引用:1難度:0.9
相似題
-
1.氮元素的化合物種類繁多,請結合以下工業制硝酸的原理示意圖,判斷下列說法不正確的是( )

A.氨合成塔中使用催化劑是為了提高合成NH3的反應速率 B.氧化爐中NH3被氧化 C.吸收塔中1molNO完全轉化成HNO3電子轉移3NA D.此路線是雷雨固氮合成硝酸的主要途徑 發布:2024/12/4 23:30:1組卷:54引用:1難度:0.6 -
2.硝酸銨是一種常用的化肥,其工業生產流程如圖,請回答下列問題。
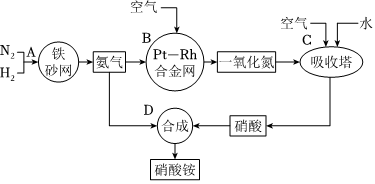
(1)寫出反應容器B中發生反應的化學方程式:。
(2)吸收塔C中通入空氣的目的是(用化學方程式解釋);C、D兩個反應容器中發生的反應,屬于氧化還原反應的是(填反應容器代號)。
(3)濃硝酸一般保存在棕色試劑瓶里,并放置在陰涼處,用化學方程式解釋原因:。
(4)碳與濃硝酸反應的化學方程式是。發布:2024/11/5 8:0:2組卷:26引用:2難度:0.9 -
3.工業上制備相關物質,涉及的反應原理及部分流程較為合理的是( )
A.制硝酸:N2 NOO2催化劑50%HNO3O2H2O濃HNO3Na(NO3)2蒸餾B.制取鎂:海水 Mg(OH)2石灰乳MgCl2溶液鹽酸Mg電解C.制碘:干海帶 浸出液H2O/浸泡碘水H2SO4/H2O2I2萃取D.制溴:濃縮海水 Br2Cl2熱空氣吹出HBr溶液SO2吸收溴蒸汽Br2Cl2發布:2024/10/9 0:0:2組卷:124引用:1難度:0.7


