 化石燃料的燃燒、硫酸工業和汽車尾氣的排放都能導致大量二氧化硫和氮氧化物排入大氣中,利用化學反應原理研究治理環境污染的方法是當前環保工作的重要研究內容之一。
化石燃料的燃燒、硫酸工業和汽車尾氣的排放都能導致大量二氧化硫和氮氧化物排入大氣中,利用化學反應原理研究治理環境污染的方法是當前環保工作的重要研究內容之一。
(1)反應2SO2(g)+O2(g)?2SΟ3(g)是硫酸工業中的重要反應,提高SO2的平衡轉化率有利于減少尾氣排放。已知該反應是放熱反應,當該反應處于平衡狀態時,在體積不變的條件下,下列措施中有利于提高SO2平衡轉化率的有BCBC(填字母)。
A.升高溫度
B.降低溫度
C.增大壓強
D.減小壓強
E.加入催化劑F.移出氧氣
(2)一定條件下,向2L密閉容器中通入2mol SO2(g)、1mol O2(g)和0.2mol SO3(g),2min后反應達到平衡時,測得SO2的轉化率為50%,則該可逆反應的平衡常數K=5.765.76;恒溫下,若向容器中再加入2mol SO2(g),則重新達到平衡時SO2的總轉化率<<50%(填“>”、“<”或“=”)。
(3)用CH4將氮氧化物(用NOx表示)催化還原為N2可以消除氮氧化物帶來的污染,請寫出總反應方程式:xCH4+4NOx═2N2+xCO2+2xH2OxCH4+4NOx═2N2+xCO2+2xH2O。
現有1L由NO2、NO組成的混合氣體,若將其還原為N2,需同溫同壓下0.4L CH4,則混合氣體中NO2、NO的物質的量之比為3:23:2。
(4)溫度為T1時在密閉容器中研究CH4催化還原氮氧化物的反應,反應過程中N2的物質的量隨時間的變化曲線如圖所示,請在圖中補畫出溫度為T2(T2>T1)時,n(N2)的變化曲線(已知該反應是放熱反應)。
【答案】BC;5.76;<;xCH4+4NOx═2N2+xCO2+2xH2O;3:2
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:9引用:1難度:0.6
相似題
-
1.反應 4A(g)+5B(g)?4C(g)+6D(g)在 5L 的密閉容器中進行,半分鐘后,C 的物質的量增 加了 0.30mol。下列敘述正確的是( )
A.容器中 D 的物質的量至少為 0.45 mol B.A 的平均反應速率是 0.010 mol?L-1?s-1 C.容器中 A、B、C、D 的物質的量之比一定是 4:5:4:6 D.容器中 A 的物質的量一定增加了 0.30 mol 發布:2024/12/30 19:30:2組卷:67引用:6難度:0.6 -
2.氫氣最早于16世紀被人工制取出來,氫氣是一種清潔能源。
(1)利用光伏電池電解水制H2是氫能的重要來源。已知:H-H鍵、O=O鍵、H-O鍵的鍵能依次為436kJ?mol-1、495kJ?mol-1、463kJ?mol-1。則2H2O(g)═2H2(g)+O2(g)△H=kJ?mol-1。
(2)T1℃時,向5L恒容密閉容器中充入0.5molCH4,只發生反應2CH4(g)?C2H4(g)+2H2(g),達到平衡時,測得c(C2H4)=2c(CH4),CH4的轉化率為;保持其他條件不變,溫度改為T2℃,經25s后達到平衡,測得c(CH4)=2c(C2H4),則0~25s內v(C2H4)=mol?L-1?s-1。
(3)CH4分解時幾種氣體的平衡分壓(pPa)的對數值lgp與溫度的關系如圖所示。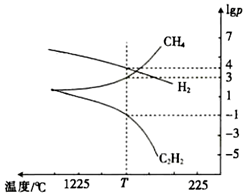
①T℃時,向一恒容密閉容器中通入一定量的CH4(g)、C2H4(g)和H2(g),只發生反應2CH4(g)?C2H2(g)+3H2(g)ΔH,ΔH(填“>”或“<”)0,此時的平衡常數Kp=(用平衡分壓代替濃度進行計算)Pa2。
②若只改變一個反應條件使Kp變大,則該條件是(填標號)。
A.減小C2H2的濃度
B.升高溫度
C.增大壓強
D.加入合適的催化劑
(4)工業上,以KNH2和液氨為電解質,以石墨為電極,電解液氨制備H2。陽極的電極反應式為,一段時間后陰、陽兩極收集到的氣體質量之比為。發布:2025/1/4 8:0:1組卷:9引用:3難度:0.5 -
3.將等物質的量的A、B混合于2L的密閉容器中,發生如下反應:3A(g)+B(g)?xC(g)+2D(g),經5min后,測得D的濃度為0.5mol/L,c(A):c(B)=3:5,C的平均反應速率為0.1mol/(L?min).求:
(1)此時A的濃度c(A)=mol/L,反應開始前容器中的A、B的物質的量:n(A)=n(B)=mol;
(2)B的平均反應速率v(B)=mol/(L?min);
(3)x的值為.發布:2024/12/30 19:0:1組卷:163引用:26難度:0.3


