 某小組同學學習了氧化還原反應的知識后,欲探究H2O2的性質:
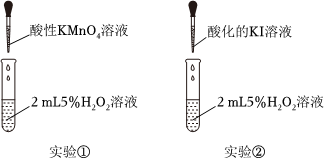
某小組同學學習了氧化還原反應的知識后,欲探究H2O2的性質:
【預測】
(1)聚焦H2O2中的核心元素O,預測H2O2既具有氧化性,也具有還原性,理由是 O的化合價為-1價,處于中間價態,既可以升高,也可以降低O的化合價為-1價,處于中間價態,既可以升高,也可以降低。
【實驗和觀察】
(2)實驗①利用了酸性高錳酸鉀的 氧化氧化性,該實驗中,證明KMnO4溶液與H2O2反應的現象除了溶液紫色褪去外,還有 有氣泡產生有氣泡產生。
(3)實驗②是為了驗證H2O2的 氧化氧化性,在反應后的溶液中加入淀粉溶液,可觀察到溶液變藍,寫出該反應的離子方程式 2I-+H2O2+2H+=I2+2H2O2I-+H2O2+2H+=I2+2H2O,并用單線橋表示電子轉移數目 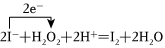
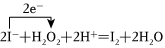 (已知:淀粉溶液遇I2會變藍)。
(已知:淀粉溶液遇I2會變藍)。
【結論】以上實驗可得出的結論是:H2O2既具有氧化性,也具有還原性。
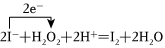
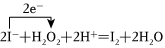
【考點】氧化還原反應的基本概念及規律.
【答案】O的化合價為-1價,處于中間價態,既可以升高,也可以降低;氧化;有氣泡產生;氧化;2I-+H2O2+2H+=I2+2H2O;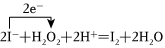
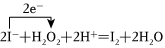
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:35引用:3難度:0.6
相似題
-
1.根據下列兩個反應判斷:2Cu+O2=2CuO,2Cu+S=Cu2S,下列敘述中錯誤的是( )
A.硫和氧氣反應中作氧化劑 B.氧氣的氧化性比硫強 C.硫的氧化性比氧氣強 D.銅是一種具有可變化合價的元素 發布:2024/12/30 14:30:1組卷:16引用:2難度:0.9 -
2.將適量的SO2通入Fe(NO3)3溶液中,溶液逐漸由棕黃色變為淺綠色,但又立即變為棕黃色,繼續滴入BaCl2溶液,產生白色沉淀。在上述一系列變化過程中,最終被還原的元素是( )
A.氮 B.硫 C.鐵 D.氧 發布:2024/12/30 14:30:1組卷:27引用:2難度:0.6 -
3.實驗證明,在一定溫度和壓強下,用銅的化合物做催化劑,甲烷(CH4)與氧氣反應只生成甲醇(CH3OH)。下列敘述正確的是( )
A.甲烷是有機物,甲醇是氧化物 B.該反應及時氧化還原反應又是化合反應 C.該反應中甲醇是還原產物,甲烷是氧化劑 D.該反應的化學方程式為CH4+O2═CH3OH 發布:2025/1/7 8:0:2組卷:2引用:1難度:0.7


