某校化學研究性學習小組通過實驗研究高爐煉鐵的化學原理,設計了如下實驗裝置:
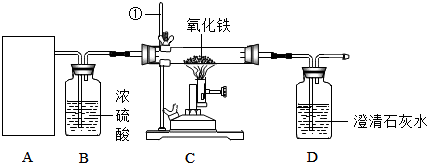
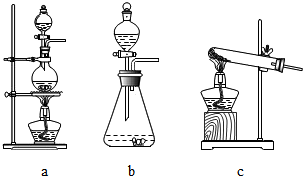
(1)已知HCOOH(甲酸) 濃H2SO4 △CO↑+H2O,根據該反應制取CO,A處應選用的氣體發生裝置是aa(填小寫字母序號);
(2)裝置中儀器①的名稱是鐵架臺鐵架臺;裝置B內所盛放濃硫酸作用是干燥CO,D裝置的作用為CO2+Ca(OH)2═CaCO3↓+H2OCO2+Ca(OH)2═CaCO3↓+H2O(用化學方程式表示)。
(3)①實驗開始時應先點燃AA(填“A”或“C”)的熱源;②反應前后C裝置玻璃管內物質顏色變化是紅色固體變為黑色紅色固體變為黑色;③C裝置玻璃管內發生反應的化學方程式為Fe2O3+3CO 高溫 2Fe+3CO2Fe2O3+3CO 高溫 2Fe+3CO2;
④檢驗C中的產物是否為鐵的方法是加稀鹽酸有氣泡產生,溶液變為淺綠色加稀鹽酸有氣泡產生,溶液變為淺綠色;
⑤待C裝置玻璃管內物質冷卻后再停止通CO的目的是待硬質粗玻璃管內物質冷卻后再停止通CO的目的是為了防止生成的鐵被氧化和澄清石灰水倒流入玻璃管內使較熱的玻璃管炸裂待硬質粗玻璃管內物質冷卻后再停止通CO的目的是為了防止生成的鐵被氧化和澄清石灰水倒流入玻璃管內使較熱的玻璃管炸裂。
(4)該裝置有一個明顯的缺陷,改進的方法為將尾氣進行點燃將尾氣進行點燃。
(5)用高爐煉鐵得到含雜質的鐵10g(雜質不溶于水,也不參加反應)與100g稀硫酸恰好完全反應,濾去雜質,得到濾液質量為108.1g,則含雜質的鐵中鐵的質量分數為84%84%。
濃
H
2
S
O
4
△
高溫
高溫
【答案】a;鐵架臺;CO2+Ca(OH)2═CaCO3↓+H2O;A;紅色固體變為黑色;Fe2O3+3CO 2Fe+3CO2;加稀鹽酸有氣泡產生,溶液變為淺綠色;待硬質粗玻璃管內物質冷卻后再停止通CO的目的是為了防止生成的鐵被氧化和澄清石灰水倒流入玻璃管內使較熱的玻璃管炸裂;將尾氣進行點燃;84%
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:103引用:2難度:0.5
相似題
-
1.某化學興趣小組用以下裝置探究煉鐵的原理.
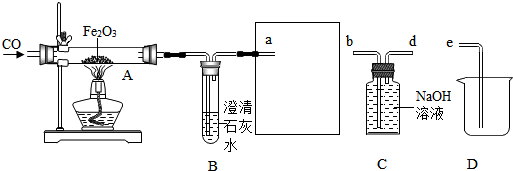
(1)加熱Fe2O3之前要先通一會兒CO,目的是.
(2)方框中連接的是C和D,導管接口的連接順序為a→()→()→(),如果導管連接錯誤,后果是.
(3)玻璃管A中發生反應的化學方程式為,用這種方法“煉”得的鐵與工業上煉出的生鐵在組成上的最大區別是.發布:2024/12/25 16:0:1組卷:202引用:5難度:0.3 -
2.甲圖是一氧化碳還原氧化鐵的裝置,乙圖是煉鐵高爐示意圖。下列敘述中正確的是( )

A.煉鐵的主要原理是:3CO+Fe2O3 2Fe+3CO2高溫B.乙圖煉鐵中原料石灰石的作用是分解制備一氧化碳 C.甲圖中實驗開始時一定要先通一段時間一氧化碳 D.乙圖中分離出爐渣后得到的生鐵是純凈物 發布:2024/12/31 8:0:1組卷:56引用:1難度:0.6 -
3.甲圖是一氧化碳還原氧化鐵的裝置,乙圖是煉鐵高爐示意圖。下列敘述中正確的是( )

A.煉鐵的主要原理是:3CO+Fe2O3═2Fe+3CO2 B.乙圖煉鐵中原料石灰石的作用是分解制備一氧化碳 C.甲圖中實驗開始時一定要先通一段時間一氧化碳 D.乙圖中分離出爐渣后得到的生鐵是純凈物 發布:2024/12/31 8:0:1組卷:230引用:2難度:0.5


