當前位置:
試題詳情
兩組同學對鐵及其化合物的性質進行探究.
(1)一組同學用圖1所示裝置對鐵與濃硫酸的反應進行實驗.已知:
2Fe+6H2SO4(濃) △ Fe2(SO4)3+3SO2↑+6H2O.請你參與探究并回答相關問題.
①檢查裝置氣密性后,將過量的鐵屑和一定量的濃硫酸放入燒瓶,塞緊橡皮塞,開始計時.t1時開始加熱,在鐵屑表面逐漸產生氣泡,當有大量氣泡產生時,控制反應溫度基本不變.甲同學將收集到的氣體體積與時間的關系粗略地表示為圖2.
在0~t1時間段,鐵屑表面沒有氣泡生成,說明鐵在濃硫酸中發生了鈍化鈍化;
t1~t2時間段,反應生成的氣體是H2、SO2H2、SO2.
②t2時,取少量反應液,先滴加少量新制飽和氯水,然后滴加KSCN溶液,呈現血紅色.若再滴加過量新制氯水,卻發現紅色褪去.同學們對紅色褪去的原因提出各自的假設.乙同學的假設是:溶液中的+3價鐵被氧化為更高的價態.你的另一種假設是溶液中的SCN-被氧化;溶液中的SCN-被氧化;;為了驗證你的假設,請設計一種簡便的實驗方案向褪色后的溶液中加入FeCl3溶液,若不恢復紅色,則我的假設成立(或:向褪色后的溶液中加入KSCN溶液,若恢復紅色,則我的假設成立)向褪色后的溶液中加入FeCl3溶液,若不恢復紅色,則我的假設成立(或:向褪色后的溶液中加入KSCN溶液,若恢復紅色,則我的假設成立).
(2)另一組同學對鐵和稀硝酸的反應進行探究.他們用a mol Fe和含有b mol HNO3的稀硝酸進行實驗,若HNO3只被還原成NO,且反應結束后溶液中含有Fe3+和Fe2+,則ab的取值范圍是14<ab<3814<ab<38;若反應結束后的溶液中n(Fe3+):n(Fe2+)=2:1,則ab的值為932932.

△
a
b
1
4
a
b
3
8
1
4
a
b
3
8
a
b
9
32
9
32
【考點】鐵及其化合物的性質實驗;氧化還原反應的計算.
【答案】鈍化;H2、SO2;溶液中的SCN-被氧化;;向褪色后的溶液中加入FeCl3溶液,若不恢復紅色,則我的假設成立(或:向褪色后的溶液中加入KSCN溶液,若恢復紅色,則我的假設成立);<<;
1
4
a
b
3
8
9
32
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/11/4 8:0:2組卷:57引用:5難度:0.1
相似題
-
 1.某同學用圖示裝置進行鐵和稀硝酸反應的實驗并進行相關的實驗探究.
1.某同學用圖示裝置進行鐵和稀硝酸反應的實驗并進行相關的實驗探究.
a.向廣口瓶內注入足量熱NaOH溶液,將盛有一定質量的純鐵粉的小燒杯放入瓶中.
b.關閉止水夾,點燃紅磷,伸入瓶中,塞好膠塞.
c.待紅磷充分燃燒,一段時間后打開分液漏斗旋塞,向燒杯中緩慢滴入一定量的4mol?L-1的稀硝酸,鐵粉完全溶解.
氣體產物成分探究
(1)實驗前如何檢查該裝置的氣密性?.
(2)燃燒紅磷的目的是.
(3)為證明氣體產物為NO,步驟c后還缺少的一步主要操作是.
產物中鐵元素價態探究:
(4)提出合理假設:
假設1:產物中只有+2價鐵;假設2:,
假設3:產物中既有+2價鐵,又有+3價鐵.
(5)設計實驗方案,驗證假設1成立(寫出實驗操作步驟現象和結論):.
問題討論:
(6)廣口瓶中熱NaOH溶液的主要作用是.若假設3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1時,則對應的離子反應方程式為.發布:2024/11/4 8:0:2組卷:64引用:5難度:0.3 -
2.鐵粉具有平肝鎮心,消癡解毒之功效,主治驚痛、癲狂、腳氣沖心、貧血等。某興趣小組探究利用反應:H2+FeCO3
Fe+CO2↑+H2O↑制取鐵粉并檢驗氣體產物實驗裝置如圖。下列說法不正確的是( )△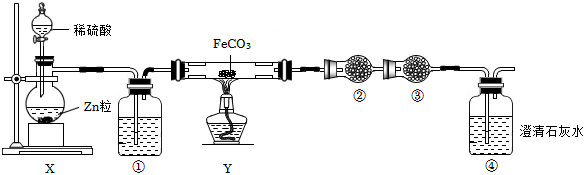
A.通過調節分液漏斗的活塞可以控制①中氣泡產生快慢 B.裝置①中的試劑是濃硫酸,目的是干燥氫氣 C.裝置②中的試劑是無水硫酸銅,目的是檢驗水蒸氣 D.為防止④中揮發的氣體進入②中干擾檢驗,③中應盛放堿石灰 發布:2024/11/17 13:0:1組卷:361引用:9難度:0.5 -
 3.硫酸亞鐵是重要的亞鐵鹽,在農業上用作農藥,主要治小麥黑穗病,還可以用作除草劑;在工業上用于染色、制造藍黑墨水和木材防腐等.
3.硫酸亞鐵是重要的亞鐵鹽,在農業上用作農藥,主要治小麥黑穗病,還可以用作除草劑;在工業上用于染色、制造藍黑墨水和木材防腐等.
(1)新制的綠礬(FeSO4?7H2O)是淺綠色的,但在空氣中極易變成黃色或鐵銹色的堿式硫酸鐵[Fe(OH)SO4],寫出該反應的化學方程式:.
(2)已知FeSO4在不同條件下分解得到產物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔點是16.8℃,沸點是44.8℃.
某研究性學習小組擬用下列裝置進行實驗探究“在加熱條件下FeSO4的分解產物”.上述裝置Ⅲ和Ⅳ用來檢驗氣體產物.試回答下列問題:
①Ⅱ裝置燒杯中水的溫度應控制在(選填“0℃、25℃、50℃”),裝置Ⅱ的作用是.
②裝置Ⅲ中的試劑可以是(選填序號,下同),現象是,則證明氣體產物中含有SO3; 裝置Ⅳ中的試劑可以是.
A.2mol?L-1Na2CO3溶液 B.品紅溶液 C.0.5mol?L-1BaCl2溶液
D.0.5mol?L-1Ba(NO3)2E.0.01mol?L-1KMnO4溶液 F.淀粉碘化鉀溶液
③裝置V中試劑為NaOH溶液,發生反應的離子方程式為.
④為了檢驗固體產物成分,取反應后的固體于試管中,加稀硫酸溶解,將所得溶液分成兩份,進行如
下實驗:
⑤若用22.8g FeSO4固體做實驗,完全分解后,得到11.2g固體,其中Fe2O3的質量分數=操作步驟 預期實驗現象 預期實驗結論 向其中一份溶液中加入 .固體中含有Fe2O3 向另一份溶液中滴加2滴黃色K3[Fe(CN)6]溶液. 產生藍色沉淀 (精確到0.1%)發布:2024/10/25 17:0:1組卷:65引用:2難度:0.7


