一氧化氮和二氧化氮是氮的兩種重要氧化物。回答下列問題:
(1)工業上處理氮氧化物時,可用濃硝酸將NO氧化為NO2,有關反應的化學方程式為 2HNO3+NO=3NO2+H2O2HNO3+NO=3NO2+H2O;再利用Na2CO3溶液吸收NO2,并通入空氣使之全部轉化為NaNO3,有關反應的化學方程式為 4NO2+2Na2CO3+O2═4NaNO3+2CO24NO2+2Na2CO3+O2═4NaNO3+2CO2。
(2)用化學方程式表示汽車尾氣中NO的產生原因:N2+O2 高溫 2NON2+O2 高溫 2NO;利用稀土金屬等催化劑能將CO和NOx轉化成無毒物質,從而減少汽車尾氣對環境的污染,該反應中氧化劑是 NOxNOx(填化學式)。
(3)為了證明NO可以與氧氣、水共同反應生成HNO3,某學生設計如圖所示裝置(夾持裝置已略去)。

①檢查裝置氣密性良好后,打開K1,關閉K2,從U形管的長管口注入稀硝酸至U形管右側膠塞下沿后,迅速關閉K1,觀察到U形管內的現象是 U形管左端液面高于右端,銅絲慢慢溶解,產生無色氣體,溶液逐漸變藍U形管左端液面高于右端,銅絲慢慢溶解,產生無色氣體,溶液逐漸變藍。
②蘸NaOH溶液棉花團的作用是 吸收氮的氧化物防止污染環境吸收氮的氧化物防止污染環境。
③打開K2,至裝置II中長玻璃管中的氣體呈無色后,打開K3,反應一段時間后,長玻璃管中并未充滿液體。設計簡單方法檢驗長玻璃管中的氣體是否為NO:再打開K3,若觀察到長玻璃管中氣體迅速變為紅棕色,則證明余氣含NO,若無顏色變化,則證明不含NO再打開K3,若觀察到長玻璃管中氣體迅速變為紅棕色,則證明余氣含NO,若無顏色變化,則證明不含NO。
高溫
高溫
【考點】氮的氧化物的性質及其對環境的影響.
【答案】2HNO3+NO=3NO2+H2O;4NO2+2Na2CO3+O2═4NaNO3+2CO2;N2+O2 2NO;NOx;U形管左端液面高于右端,銅絲慢慢溶解,產生無色氣體,溶液逐漸變藍;吸收氮的氧化物防止污染環境;再打開K3,若觀察到長玻璃管中氣體迅速變為紅棕色,則證明余氣含NO,若無顏色變化,則證明不含NO
高溫
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:20引用:1難度:0.6
相似題
-
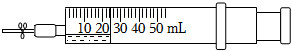 1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
1.如圖所示,在一支50mL的注射器里充入20mL NO,然后吸入5mL水,用乳膠管和彈簧夾封住管口。
(1)根據操作步驟,完成表格:
(2)如果要將注射器中的NO充分轉化,可以采取什么措施?操作步驟河 實驗現象 解釋原因 Ⅰ.振蕩注射器,觀察現象 無明顯現象 ① Ⅱ.打開彈簧夾,快速吸入10mL空氣后夾上彈簧夾,觀察現象 ② ③ Ⅲ.振蕩注射器,再觀察現象 氣體又變為無色,注射器的活塞向內移動 ④ 。
(3)上述實驗對工業上生產硝酸有什么啟示?。發布:2024/12/30 6:30:2組卷:9引用:3難度:0.6 -
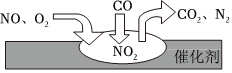 2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )
2.隨著我國汽車年銷量的大幅增加,空氣環境受到了很大的污染。汽車尾氣凈化裝置里,氣體在催化劑表面吸附與解吸作用的過程如圖所示,下列說法正確的是( )A.該轉化過程中N元素化合價降低,C元素化合價升高,共兩種元素化合價發生變化 B.汽車尾氣的主要污染成分包括CO、NO和N2 C.NO和O2必須在催化劑表面才能反應 D.催化轉化的總化學方程式為2NO+O2+4CO 4CO2+N2催化劑發布:2024/12/30 6:30:2組卷:9引用:2難度:0.6 -
3.下列有關NO2的敘述正確的是( )
A.閃電時,空氣中的N2和O2可直接化合生成NO2 B.NO2與水反應時,NO2作還原劑,水作氧化劑 C.NO2、NO都是大氣污染氣體,在空氣中都能穩定存在 D.NO2是紅棕色有毒氣體 發布:2024/12/30 6:30:2組卷:7引用:2難度:0.7


