離子反應(yīng)是中學(xué)化學(xué)中重要的反應(yīng)類型。
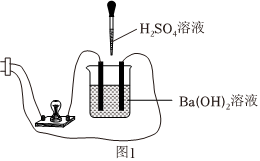
【實(shí)驗(yàn)】某學(xué)習(xí)小組為證實(shí)Ba(OH)2溶液和H2SO4溶液的反應(yīng)是離子反應(yīng),設(shè)計(jì)如圖1所示實(shí)驗(yàn):
(1)完成下表空白處。
| 實(shí)驗(yàn)步驟 | 實(shí)驗(yàn)現(xiàn)象 | 實(shí)驗(yàn)結(jié)論 |
| 連接好裝置,向燒杯中加入25mL一定濃度的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加一定濃度的H2SO4溶液直至過(guò)量,邊滴加邊振蕩 | 產(chǎn)生白色沉淀, 溶液由紅色變?yōu)闊o(wú)色;燈泡由明變暗,直至熄滅,然后又逐漸變亮 溶液由紅色變?yōu)闊o(wú)色;燈泡由明變暗,直至熄滅,然后又逐漸變亮 |
Ba(OH)2溶液和H2SO4溶液的反應(yīng)是離子反應(yīng) |
Ba2++2OH-+2H++=BaSO4↓+2H2O
SO
2
-
4
Ba2++2OH-+2H++=BaSO4↓+2H2O
。SO
2
-
4
【實(shí)驗(yàn)拓展】已知某無(wú)色透明溶液中可能含有下列離子中的若干種:K+、Mg2+、Fe3+、Ba2+、
SO
2
-
4
CO
2
-
3
Ⅰ.取少量原溶液,滴入紫色石蕊試液,溶液呈藍(lán)色;
Ⅱ.取少量原溶液,滴入BaCl2溶液,無(wú)明顯現(xiàn)象;
Ⅲ.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀產(chǎn)生;
Ⅳ.取少量原溶液,滴入少量稀H2SO4,有白色沉淀產(chǎn)生。
(3)某同學(xué)提出,不用通過(guò)實(shí)驗(yàn)即可判斷出原溶液中不存在的離子是
Fe3+
Fe3+
(填離子符號(hào),下同)。(4)由Ⅱ可以判斷出原溶液中不存在的離子是
SO
2
-
4
CO
2
-
3
SO
2
-
4
CO
2
-
3
(5)Ⅲ是為了判斷
Cl-
Cl-
離子的存在,先滴加足量稀硝酸的目的是 排除OH-的干擾
排除OH-的干擾
。寫出Ⅲ中發(fā)生反應(yīng)的離子方程式 H++OH-=H2O或Cl-+Ag+=AgCl↓
H++OH-=H2O或Cl-+Ag+=AgCl↓
(寫一個(gè)即可)。(6)由Ⅳ可以判斷出溶液中含有的離子是
Ba2+
Ba2+
(填離子符號(hào))。【考點(diǎn)】常見(jiàn)離子的檢驗(yàn)方法;離子反應(yīng)發(fā)生的條件.
【答案】溶液由紅色變?yōu)闊o(wú)色;燈泡由明變暗,直至熄滅,然后又逐漸變亮;Ba2++2OH-+2H++=BaSO4↓+2H2O;Fe3+;、;Cl-;排除OH-的干擾;H++OH-=H2O或Cl-+Ag+=AgCl↓;Ba2+
SO
2
-
4
SO
2
-
4
CO
2
-
3
【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/4/20 14:35:0組卷:47引用:2難度:0.6
相似題
-
1.某無(wú)色溶液,其中可能存在Na+、Ba2+、
、S2-、AlO-2、SO2-3.取該溶液進(jìn)行有關(guān)實(shí)驗(yàn),實(shí)驗(yàn)結(jié)果如圖所示.SO2-4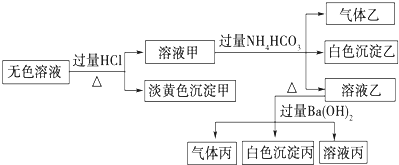
回答下列問(wèn)題:
(1)沉淀甲的化學(xué)式為.
(2)由溶液甲生成沉淀乙的離子方程式為.
(3)沉淀丙中一定含有(填化學(xué)式,下同),可能含有.
(4)綜合上述信息,該溶液中肯定存在的離子有.
(5)該溶液顯性(填酸性、堿性或中性),若要檢驗(yàn)其酸堿性,下圖操作正確的是.
請(qǐng)用離子方程式表示顯堿性的原因:.發(fā)布:2024/12/30 6:0:2組卷:10引用:2難度:0.3 -
2.在實(shí)驗(yàn)室鑒定氯酸鉀晶體和1-氯丙烷中的氯元素,現(xiàn)設(shè)計(jì)了下列實(shí)驗(yàn)操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加熱;④加催化劑MnO2;⑤加蒸餾水過(guò)濾后取濾液;⑥過(guò)濾后取殘?jiān)虎哂肏NO3酸化。(填序號(hào))
(1)鑒定氯酸鉀中氯元素的操作步驟依次是
(2)鑒定1-氯丙烷中氯元素的操作步驟依次是。發(fā)布:2024/12/30 8:0:15組卷:67引用:8難度:0.5 -
3.為檢驗(yàn)?zāi)撤N陽(yáng)離子為Na-的溶液中含有的陰離子是SO42-、CO32-、OH-還是Cl-,下列設(shè)計(jì)的方案合理的是( )
A.檢驗(yàn)CO32-:向待測(cè)液中加入足量的鹽酸產(chǎn)生氣泡,將氣體通入濃Ba(OH)2溶液中有白色沉淀生成 B.檢驗(yàn)SO42-:先向待測(cè)液中加入鹽酸至溶液呈酸性,未見(jiàn)沉淀或氣體生成,再加入BaCl2溶液出現(xiàn)白色沉淀 C.檢驗(yàn)OH-:向待測(cè)液中加入石蕊溶液,溶液變紅 D.檢驗(yàn)Cl-:向待測(cè)液中依次加入AgNO3溶液和稀鹽酸,有白色渾濁出現(xiàn) 發(fā)布:2024/12/30 6:30:2組卷:9引用:2難度:0.6
相關(guān)試卷


