酸和堿反應是一類重要的化學反應。某同學利用圖1實驗研究稀鹽酸與氫氧化鈉溶液反應的過程,并測量反應過程中溶液的pH和溫度的變化情況,得到圖2和圖3,請回答下列問題:
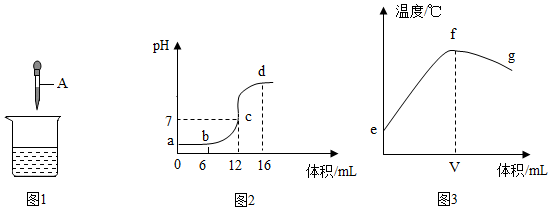
(1)膠頭滴管中A溶液的溶質是:NaOHNaOH(填化學式)。
(2)要配制50克15%的稀鹽酸,需要質量分數(shù)為30%的濃鹽酸2525克。
(3)該興趣小組同學推斷出圖3中V的值為12,他的理由是:由圖2可知,恰好完全反應時消耗氫氧化鈉溶液體積是12mL,說明此時放熱最多,溫度最高由圖2可知,恰好完全反應時消耗氫氧化鈉溶液體積是12mL,說明此時放熱最多,溫度最高。
(4)下列說法正確的是ADAD。
A.圖2中b點所示溶液中的溶質是NaCl和HCl
B.取圖2中d點所示溶液加熱蒸干所得固體為純凈物
C.圖2中c→d所示溶液中NaCl的質量不斷增加
D.圖3中e→f變化趨勢可說明該反應是放熱反應
【答案】NaOH;25;由圖2可知,恰好完全反應時消耗氫氧化鈉溶液體積是12mL,說明此時放熱最多,溫度最高;AD
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經書面同意,不得復制發(fā)布。
發(fā)布:2024/11/30 12:30:1組卷:337引用:5難度:0.5
相似題
-
1.電導率是衡量溶液導電能力大小的物理量,在相同條件下,電導率與離子濃度(單位體積內的離子數(shù))成正比,鹽酸和氫氧化鈉反應電導率曲線如圖所示,以下分析不正確的是( )
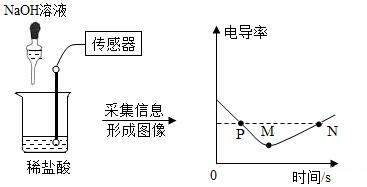
A.電導率減小可能是由于溶液中離子數(shù)量逐漸減小 B.M點時NaOH溶液與稀鹽酸恰好完全反應 C.N點時溶液中的離子數(shù)大于P點 D.該實驗證明溶液中始終含有帶電的粒子 發(fā)布:2024/12/28 15:30:1組卷:78引用:6難度:0.5 -
2.向盛有50g 10% Ba(OH)2溶液的燒杯中慢慢滴加稀硫酸至過量,如圖(縱坐標表示燒杯中其他量的變化)所有有關量的變化與所加入稀硫酸質量的關系錯誤的是( )
A. 
B. 
C. 
D.  發(fā)布:2024/12/28 15:30:1組卷:15引用:4難度:0.5
發(fā)布:2024/12/28 15:30:1組卷:15引用:4難度:0.5 -
3.等質量的氫氧化鈉溶液和稀鹽酸混合后,若所得溶液pH=7,則( )
A.所用氫氧化鈉溶液和稀鹽酸的溶質質量分數(shù)相等 B.混合溶液中鈉離子與氯離子個數(shù)相等 C.混合前后水分子總數(shù)不變 D.混合前后陽離子總數(shù)不變 發(fā)布:2024/12/28 15:0:1組卷:134引用:10難度:0.5


