CO是一種重要的含碳化合物,它與生產、生活息息相關。
(1)汽車尾氣中CO、NO2在一定條件下可發生反應:4CO(g)+2NO2(g)?4CO2(g)+N2(g),一定溫度下,向容積固定的2L的密閉容器中充入一定量的CO和NO2,反應經10min達到化學平衡。CO的物質的量隨時間的變化曲線如圖1所示:
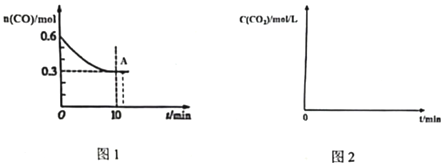
①0~10min內該反應的平均反應速率v(CO)=0.015mol/(L?min)0.015mol/(L?min);
②A點的v正(NO2) ==v逆(NO2)(填“>”“<”或“=”);
③下列不能說明該反應一定達到化學平衡的是 CDCD(填序號);
A.單位時間內,每消耗4mol CO2的同時生成1mol N2
B.NO2在該條件下達到最大轉化率
C.容器內混合氣體密度保持不變
D.c(CO):c(NO2):c(CO2):c(N2)=4:2:4:1
④在圖2中畫出0~15min時間內,CO2的濃度隨時間變化的曲線圖為
 。
。
(2)一氧化碳一氧燃料電池是使用CO制造成儲存能量的電池,其總反應方程式為:2CO+O2═2CO2,一氧化碳一氧燃料電池在酸性條件下放電時,正極的電極反應式:O2+4e-+4H+=2H2OO2+4e-+4H+=2H2O。


【考點】化學平衡狀態的判斷;原電池與電解池的綜合.
【答案】0.015mol/(L?min);=;CD; ;O2+4e-+4H+=2H2O
;O2+4e-+4H+=2H2O
 ;O2+4e-+4H+=2H2O
;O2+4e-+4H+=2H2O【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:22引用:1難度:0.6
相似題
-
1.在一定溫度下的定容容器中,當下列哪些物理量不再發生變化時,表明反應A(g)+2B(g)?C(g)+D(g)已達到平衡狀態( )
①混合氣體的壓強
②混合氣體的密度
③B的物質的量濃度
④混合氣體的總物質的量
⑤混合氣體的平均相對分子質量
⑥v(C)與v(D)的比值
⑦混合氣體的總質量.A.②③④⑤⑥⑦ B.①③④⑤ C.①②③④⑤⑦ D.①③⑤ 發布:2024/12/30 19:30:2組卷:40引用:3難度:0.7 -
2.二甲醚(DME)一種清潔的替代燃料,不含硫,不會形成微粒,而且與汽油相比,排放的NO2更少,因此是優良的柴油機替代燃料。工業上利用一步法合成二甲醚的反應如下(復合催化劑為CuO/ZnO/Al2O2):
2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol
(1)若反應在恒溫、恒壓下進行,以下敘述能說明該反應達到平衡狀態的是
A.CO和H2的物質的量濃度比是1:2
B.CO的消耗速率等于CH3OCH3的生成速率的2倍
C.容器中混合氣體的體積保持不變
D.容器中混合氣體的平均摩爾質量保持不變
E.容器中混合氣體的密度保持不變
(2)600℃時,一步法合成二甲醚過程如下:
CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ/mol
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2
CO(g)+H2O(g)═CO2(g)+H2(g)△H3=-38.7kJ/mol
則△H2=。
(3)復合催化劑的制備方法之一是Na2CO3共沉淀法:制備1mol/L的硝酸銅,硝酸鋅和硝酸鋁的水溶液。然后向盛有去離子水的燒杯中同時滴加混合硝酸鹽溶液和1mol/L的Na2CO3水溶液,70℃下攪拌混合。沉淀后過濾,洗滌沉淀物,80℃下干燥12小時,然后500℃下焙燒16小時。
請寫出上述過程中硝酸鋁與Na2 CO3水溶液反應的離子方程式:
(4)以DME為燃料,氧氣為氧化劑,在酸性電解質溶液中用惰性電極制成燃料電池,則通入氧氣的電極是電源的(填正、負)極,通DME的電極反應為。發布:2025/1/3 8:0:1組卷:18引用:1難度:0.5 -
3.在一定溫度下的定容容器中,反應:A(s)+2B(g)?C(g)+D(g)。下列不能表明反應達到平衡狀態的是( )
A.氣體的壓強不變 B.氣體平均相對分子質量不變 C.v生成(B)═2v生成(C) D.B物質的物質的量濃度不變 發布:2024/12/30 19:0:1組卷:110引用:4難度:0.8


