某反應(yīng)中反應(yīng)物與生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一種未知物質(zhì)X。
(1)已知KBrO3在反應(yīng)中得到電子,則該反應(yīng)的還原劑是AsH3AsH3。
(2)已知2個(gè)KBrO3在反應(yīng)中得到10個(gè)電子生成X,則X的化學(xué)式為Br2Br2。
(3)根據(jù)上述反應(yīng)可推知bdbd(填序號(hào))。
a.氧化性:H3AsO4>KBrO3
b.氧化性:KBrO3>H3AsO4
c.還原性:X>AsH3
d.還原性:AsH3>X
(4)將氧化劑和還原劑的化學(xué)式及其配平后的化學(xué)計(jì)量數(shù)填入下列橫線中,并標(biāo)出電子轉(zhuǎn)移的方向和數(shù)目
 。
。


【答案】AsH3;Br2;bd;

【解答】
【點(diǎn)評(píng)】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復(fù)制發(fā)布。
發(fā)布:2024/5/27 14:0:0組卷:25引用:1難度:0.7
相似題
-
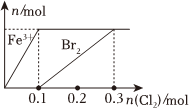 1.向200mLFeBr2溶液中逐漸通入Cl2,其中n(Fe3+)、n(Br2 )隨通入n(Cl2)的變化如圖所示,下列說法錯(cuò)誤的是( )
1.向200mLFeBr2溶液中逐漸通入Cl2,其中n(Fe3+)、n(Br2 )隨通入n(Cl2)的變化如圖所示,下列說法錯(cuò)誤的是( )A.還原性強(qiáng)弱:Fe2+>Br- B.由圖可知,該FeBr2溶液的濃度為1mol?L-1 C.n(Cl2)=0.12mol時(shí),溶液中的離子濃度有 ═c(Fe3+)c(Br-)59D.氯氣過量時(shí),反應(yīng)的離子方程式為:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- 發(fā)布:2024/12/7 9:30:1組卷:50引用:3難度:0.5 -
2.根據(jù)反應(yīng)式:①2Fe3++2I-═2Fe2++I2,②Br2+2Fe2+═2Br-+2Fe3+,可判斷離子的還原性從強(qiáng)到弱的順序是( )
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br- 發(fā)布:2024/11/28 12:30:2組卷:346引用:8難度:0.8 -
3.已知:
①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;
②Cl2+2FeCl2═2FeCl3;
③2KI+2FeCl3═2KCl+I2+2FeCl2。
則下列判斷正確的是( )A.氧化性:MnO4->Fe3+>Cl2>I2 B.還原性:Cl->I->Fe2+ C.Fe3+只有氧化性,F(xiàn)e2+只有還原性 D.由信息推測:Cl2+2I-═2Cl-+I2反應(yīng)可以進(jìn)行 發(fā)布:2024/12/11 14:0:2組卷:421引用:7難度:0.4


