 鎳具有優良的物理和化學特性,是許多領域尤其是高技術產業的重要原料.羰基法提純粗鎳涉及的兩步反應依次為:
鎳具有優良的物理和化學特性,是許多領域尤其是高技術產業的重要原料.羰基法提純粗鎳涉及的兩步反應依次為:
①Ni(S)+4CO(g)50℃Ni(CO)4(g)+Q;
②Ni(CO)4(g)230℃Ni(S)+4CO(g)完成下列填空:
(1)在溫度不變的情況下,要提高反應(1)中Ni(CO)4的產率,可采取的措施有增大壓強增大壓強、從反應體系中移走Ni(CO)4(g)從反應體系中移走Ni(CO)4(g).
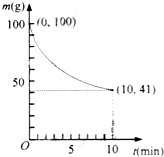
(2)已知在一定條件下的2L密閉容器中制備Ni(CO)4,粗鎳(純度98.5%,所含雜質不與CO反應)剩余質量和反應時間的關系如圖所示.Ni(CO)4在0~10min的平均反應速率為0.05mol/(L?min)0.05mol/(L?min).
(3)若反應(2)達到平衡后,保持其他條件不變,降低溫度,重新達到平衡時bcbc.
a.平衡常數K增大 b.CO的濃度減小
c.Ni的質量減小 d.v逆[Ni(CO)4]增大.
(4)簡述羰基法提純粗鎳的操作過程:在封閉的玻璃管一端放入粗鎳,控制溫度在50℃,通入CO氣體,一點時間后在玻璃管的另一端加熱至230℃,即可在該端獲得純凈的鎳.在封閉的玻璃管一端放入粗鎳,控制溫度在50℃,通入CO氣體,一點時間后在玻璃管的另一端加熱至230℃,即可在該端獲得純凈的鎳..
50
℃
230
℃
【考點】化學平衡的影響因素;反應速率的定量表示方法.
【答案】增大壓強;從反應體系中移走Ni(CO)4(g);0.05mol/(L?min);bc;在封閉的玻璃管一端放入粗鎳,控制溫度在50℃,通入CO氣體,一點時間后在玻璃管的另一端加熱至230℃,即可在該端獲得純凈的鎳.
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:641引用:15難度:0.1
相似題
-
1.升高溫度,下列數據不一定增大的是( )
A.化學反應速率v B.水的離子積常數Kw C.化學平衡常數K D.氨水的電離平衡常數Ka 發布:2025/1/6 6:0:5組卷:31引用:4難度:0.7 -
2.催化還原CO2是解決溫室效應及能源問題的重要手段之一。研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發生以下兩個平衡反應。下列有關說法不正確的是( )
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-53.7kJ?mol-1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2=+41.2kJ?mol-1A.反應①為放熱反應,反應②為吸熱反應 B.使用不同催化劑,會改變反應①②的△H C.反應CO(g)+2H2(g)?CH3OH(g)的△H3=-94.9kJ?mol-1 D.投料比不變,增加反應物的濃度可提高CO2轉化為CH3OH平衡轉化率 發布:2025/1/6 6:0:5組卷:90引用:3難度:0.5 -
3.現代工業將煤汽化,既可以提高燃料的利用率、減少CO、SO2等的排放,又可以擴大水煤氣的用途.甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上一般可采用水煤氣來合成甲醇CO(g)+2H2(g)?CH3OH(g).
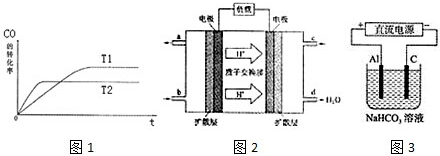
(1)如圖1是該反應在不同溫度下CO的轉化率隨時間變化的曲線.
①T1和T2溫度下的平衡常數大小關系是K1K2(填“>”、“<”或“=”).
②以下有關說法正確的是
a.恒溫、恒容條件下,容器內的壓強不發生變化則可逆反應達到平衡
b.一定條件下,H2的消耗速率是CO的消耗速率的2倍時可逆反應達到平衡
c.使用合適的催化劑能縮短達到平衡的時間并提高CH3OH的產率
d.某溫度下,將2molCO和6molH2充入2L的密閉容器中,充分反應,達到平衡后,測得c(CO)=0.2mol/L,則CO的轉化率為80%
(2)已知在常溫常壓下①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H=-akJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-bkJ?mol-1③H2O(g)=H2O(1)△H=-ckJ?mol-1
則:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=kJ?mol-1
(3)2009年10月,中國科學院長春應用化學研究所在甲醇燃料電池技術方面獲得新突破,組裝出了自呼吸電池及主動式電堆.甲醇燃料電池的工作原理如圖2所示.
①該電池正極的電極反應式為.
②工作一段時間后,當6.4g甲醇完全反應生成CO2時,有個電子發生轉移.
(4)以上述電池做電源,用圖3所示裝置,在實驗室中模擬鋁制品面“鈍化”處理的過程中,發現溶液逐漸變渾濁,原因是、(用相關的電極反應式和離子方程式表示)發布:2024/12/30 14:0:1組卷:26引用:3難度:0.5


