1774年,舍勒在研究軟錳礦(主要成分MnO2)時,將它與濃鹽酸混合加熱,產(chǎn)生了一種黃綠色氣體。舍勒的方法沿用至今,實驗室用如圖裝置制取氯氣并進行氯氣性質(zhì)探究。
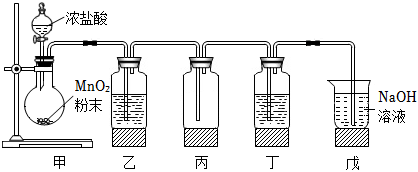
完成下列填空。
(1)甲為發(fā)生裝置,該處還缺少的玻璃儀器是 酒精燈酒精燈。盛放濃鹽酸的儀器名稱為 分液漏斗分液漏斗。
(2)乙為除雜裝置,盛有 bb(填寫下列字母編號),目的是 除去氯氣中的氯化氫氣體除去氯氣中的氯化氫氣體。
a.堿石灰
b.飽和食鹽水
c.濃硫酸
d.飽和碳酸氫鈉溶液
e.四氯化碳
(3)檢驗丙裝置中氯氣是否已集滿的操作是 將潤濕的淀粉-KI試紙接近集氣瓶口,試紙變藍則已收集滿將潤濕的淀粉-KI試紙接近集氣瓶口,試紙變藍則已收集滿。
(4)丁裝置中盛有紫色石蕊試液,實驗中可觀察到溶液顏色發(fā)生了如下變化。請完成下表中的三處空白。
| 實驗現(xiàn)象 | 原因 |
| 最初溶液從紫色逐漸變?yōu)? 紅 紅 色 |
氯氣與水反應生成的H+使石蕊變色 |
| 隨后溶液逐漸變?yōu)闊o色 |
氯氣與水反應生成的HClO將石蕊氧化為無色物質(zhì) 氯氣與水反應生成的HClO將石蕊氧化為無色物質(zhì)
|
| 然后溶液從無色逐漸變?yōu)? 淡黃綠 淡黃綠 色 |
/ |
吸收未反應的氯氣,防止污染空氣
吸收未反應的氯氣,防止污染空氣
,該處的化學反應方程式為 Cl2+2NaOH=NaClO+NaCl+H2O
Cl2+2NaOH=NaClO+NaCl+H2O
。(6)實驗結(jié)束,測得戊裝置中溶液質(zhì)量為200g,NaOH溶液的質(zhì)量分數(shù)由30%減小到1%,則吸收的氯氣質(zhì)量是
40.7
40.7
g(保留一位小數(shù))。【考點】氯氣的實驗室制法.
【答案】酒精燈;分液漏斗;b;除去氯氣中的氯化氫氣體;將潤濕的淀粉-KI試紙接近集氣瓶口,試紙變藍則已收集滿;紅;氯氣與水反應生成的HClO將石蕊氧化為無色物質(zhì);淡黃綠;吸收未反應的氯氣,防止污染空氣;Cl2+2NaOH=NaClO+NaCl+H2O;40.7
【解答】
【點評】
聲明:本試題解析著作權屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:32引用:1難度:0.6
相似題
-
1.為了驗證干燥的氯氣無漂白性,濕潤的氯氣具有漂白性,某同學設計實驗如圖.其中B、C、D、E、F分別盛有飽和食鹽水、濃硫酸.干燥紅色布條、濃硫酸、濕潤紅色布條.
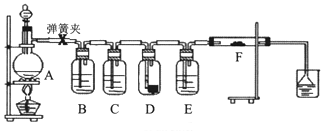
請回答:
(1)E中濃硫酸的作用.
(2)將F中的濕潤布條換成卷曲的細銅絲,并用酒精燈加熱,可看到的現(xiàn)象是.
(3)若用裝置A制取2.24L(標況)氯氣,消耗10mol/L濃鹽酸的體積明顯大于40mL,造成該結(jié)果的可能原因有.
A.濃鹽酸的揮發(fā) B.隨反應進行鹽酸濃度下降
C.加熱時火力不夠猛 D.MnO2固體過量.發(fā)布:2025/1/15 8:0:2組卷:17引用:1難度:0.3 -
2.如圖是某同學設計的氯氣制備及性質(zhì)驗證實驗裝置。相關說法正確的是( )

A.脫脂棉中的無水氯化鈣可以用堿石灰代替 B.該實驗裝置可證明干燥的氯氣沒有漂白作用 C.濕潤的紫色石蕊試紙變紅色,說明反應生成了酸性物質(zhì) D.濕潤的淀粉碘化鉀試紙變藍色,然后又逐漸褪去,說明氯氣具有漂白性 發(fā)布:2025/1/15 8:0:2組卷:20引用:2難度:0.8 -
3.實驗室中模擬用甲烷與氯氣反應得到的副產(chǎn)品來制取鹽酸,原理如圖,下列說法不正確的是( )
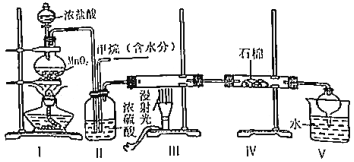
A.依據(jù)裝管Ⅰ中的現(xiàn)象控制氣流的速度 B.分離裝置V中鹽酸的最佳操作方法是分液 C.裝置Ⅳ的石棉中可加入一些氫氧化鈉粉末 D.實驗過程中可觀察到裝置Ⅲ中硬質(zhì)玻璃管內(nèi)壁有附著的油珠 發(fā)布:2024/12/30 17:0:5組卷:61引用:1難度:0.7


