 (1)有下列物質 ①Cu;②液氨;③CH3COOH;④NaHCO3;⑤H2O;⑥熔融NaCl;⑦NH3?H2O;⑧NH4Cl屬于弱電解質的是 ③⑤⑦③⑤⑦(填序號)
(1)有下列物質 ①Cu;②液氨;③CH3COOH;④NaHCO3;⑤H2O;⑥熔融NaCl;⑦NH3?H2O;⑧NH4Cl屬于弱電解質的是 ③⑤⑦③⑤⑦(填序號)
| 化學式 | NH3?H2O | HCN | CH3COOH | H2CO3 |
| 電離平衡常數(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
CH3COOH>H2CO3>HCN
CH3COOH>H2CO3>HCN
(3)鹽類水解程度的強弱同樣與弱電解質的電離程度有一定聯系,結合表中數據回答下列問題:
①25℃時,有等濃度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三種溶液的pH由大到小的順序為
b>a>c
b>a>c
.(填溶液前序號)②濃度相同的NaCN溶液與CH3COOK溶液相比,c(Na+)-c(CN-)
>
>
c(K+)-c(CH3COO-).(填“>”、“<”或“=”)③將等體積等物質的量濃度的鹽酸和氨水混合后,溶液呈
酸
酸
性(填“酸”、“堿”或“中”),用離子方程式表示原因 NH
+
4
NH
+
4
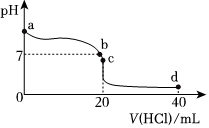
④室溫下,若將0.1mol?L-1鹽酸滴入20mL 0.1mol?L-1氨水中,溶液pH隨加入鹽酸體積的變化曲線如圖所示.b點所示溶液中的溶質是
NH3?H2O、NH4Cl
NH3?H2O、NH4Cl
.⑤NH4HCO3溶液呈
堿
堿
性(填“酸”、“堿”或“中”).(4)結合表中數據,向NaCN溶液中通入少量CO2,所發生反應的化學方程式
NaCN+H2O+CO2=HCN+NaHCO3
NaCN+H2O+CO2=HCN+NaHCO3
.【考點】鹽類水解的應用.
【答案】③⑤⑦;CH3COOH>H2CO3>HCN;b>a>c;>;酸;+H2O?NH3?H2O+H+;NH3?H2O、NH4Cl;堿;NaCN+H2O+CO2=HCN+NaHCO3
NH
+
4
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/6/27 10:35:59組卷:39引用:3難度:0.5
相似題
-
1.下列鹽的水溶液,其pH值小于7的是( )
A.NH4Cl溶液 B.NaCl溶液 C.Na2SO4溶液 D.NaHCO3溶液 發布:2024/12/20 8:0:1組卷:25引用:6難度:0.9 -
2.已知Mg2C3的結構與CaC2的結構相似.由此可斷定Mg2C3與水反應的產物是( )
A.Mg(OH)2和CH≡CH B.Mg(OH)2和CH4 C.Mg(OH)2和CH3C≡CH D.Mg(OH)2和CH3CH=CH2 發布:2024/12/30 8:0:15組卷:52引用:6難度:0.7 -
3.下列生活現象其對應的化學原理的說法正確的是( )
A.明礬可以起到凈水消毒作用 B.豆漿膠體聚沉說明了膠體在一定條件下可以轉化為濁液 C.蔬菜中含有還原性的維生素C,為了保證營養價值,烹飪時應當文火慢燉而不是爆炒 D.月餅中的防腐劑含有氯化鈣,主要起到吸收氧氣防止氧化的作用 發布:2024/12/27 8:0:2組卷:24引用:1難度:0.6


